题目内容
下图是两种盐酸与铁铬合金的反应随铬(Cr)的质量分数变化的实验结果(铬与盐酸反应)下列说法错的是
- A.稀硫酸、稀盐酸中的阳离子都是H+
- B.图中的“5%”表示酸溶液中溶质的质量分数
- C.同一种酸与铁铬合金反应的速度随着Cr质量分数的增加一直加快
- D.与相同铁铬合金反应,5%硫酸比5%的盐酸反应快
A、电离出来的阳离子都是氢离子的化合物是酸,盐酸和硫酸都是酸,故A说法正确;
B、图中的“5%”就是表示酸溶液中溶质的质量分数,故B说法正确;
C、由图示可知有一段反应铬的质量分数在减小,故C说法错误;
D、在图示的纵坐标表示反应速度,并且硫酸的曲线在盐酸的曲线上面,所以5%硫酸比5%盐酸反应快,故D说法正确.
故选C.

 习题精选系列答案
习题精选系列答案金属是一种重要的材料,人类的生活和生产都离不开金属,高科技新材料的开发和应用也需要金属。下图表示了金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限。
(1)根据图中数据和有关的化学知识,你认为金属大规模开发、利用的先后顺序跟下列哪些因素有关(填序号)
①地壳中金属元素的含量 ②金属的导电性 ③金属的活动性
④金属的延展性 ⑤金属冶炼的难易程度
(2)钢铁的生产和使用是人类文明和社会进步的一个重要标志。请你写出一氧化碳在高温条件下把铁从赤铁矿(主要成分是氧化铁)里还原出来的化学方程式
能证明产物中有铁粉的方法是: 。
(3)每年世界上钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟 等物质相互作用的结果。试举两种减缓钢铁锈蚀的方法:① ② ;工人师傅在焊接钢铁制品时,通常先用稀盐酸清洗制品,原因是(用方程式表示) 。
(4)铝的活动性比铁强,但铝在空气中却表现出良好的抗蚀性,其原因是什么?(用方程式表示)
(5)日常使用的金属材料多数属于合金。下表列出了一些常见合金的主要成分和性能。
由右表可推断,与组成合金的纯金属相比,合金的优点一般有(填编号) :①强度更好②硬度更大③熔点更低④抗腐蚀性能更优良
| 合金 | 合金的主要性能 | 主要成分及纯金属的性能 |
| 焊锡 | 熔点183℃ | 锡:熔点232℃;铅:熔点327℃。 |
| 硬铝 | 强度和硬度好 | 铝、铜、镁等。硬度小,质软。 |
| 不锈钢 | 抗腐蚀性好 | 铁、铬、镍等。纯铁易生锈。 |
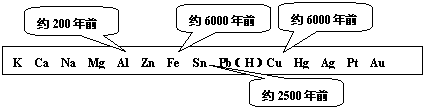 |
金属是一种重要的材
 料,人类的生活和生产都离不开金属,高科技新材料的开发和应用也需要金属。下图表示了金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限。
料,人类的生活和生产都离不开金属,高科技新材料的开发和应用也需要金属。下图表示了金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限。 (1)根据图中数据和有关的化学知识,你认为金属大规模开发、利用的先后顺序跟下列哪些因素有关(填序号) 
①地壳中金属元素的含量 ②金属的导电性 ③金属的活动性
④金属的延展性 ⑤金属冶炼的难易程度
(2)钢铁的生产和使用是人类文明和社会进步的一个重要标志。请你写出一氧化碳在高温条 件下把铁从赤铁矿(主要成分是氧化铁)里还原出来的化学方程式
件下把铁从赤铁矿(主要成分是氧化铁)里还原出来的化学方程式 
能证明产物中有铁粉的方法是: 。
(3)每年世界上钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟 等物质相互作用的结果。试举两种减缓钢铁锈蚀的方法:① ② ;工人师傅在焊接钢铁制品时,通常先用稀盐酸清洗制品,原因是(用方程式表示) 。
(4)铝的活动性比铁强,但铝在空气中却表现出良好的抗蚀性,其原因是什么?(用方程式表示)
(5)日常使用的金属材料多数属于合金。下表列出了一些常见合金的主要成分和性能。
由右表可推断,与组成合金的纯金属相比,合金的优点一般有(填编号) :①强度更好②硬度更大③熔点更低④抗腐蚀性能更优良
| 合金 | 合金的主要性能 | 主要成分及纯金属的性能 |
| 焊锡 | 熔点183℃ | 锡:熔点232℃;铅:熔点327℃。 |
| 硬铝 | 强度和硬度好 | 铝、铜、镁等。硬度小,质软。 |
| 不锈钢 | 抗腐蚀性好 | 铁、铬、镍等。纯铁易生锈。 |