题目内容
下列图象分别对应四种操作过程,其中不正确的是( )
A、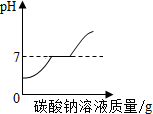 向HCl和CaCl2的混合溶液中不断加入Na2CO3溶液 |
B、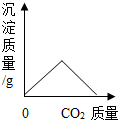 向氢氧化钙溶液中不断通入CO2气体 |
C、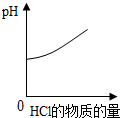 稀盐酸滴入碳酸钠溶液 |
D、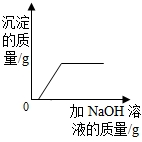 向盐酸和氯化铁的混合溶液中加入氢氧化钠溶液 |
考点:盐的化学性质,酸的化学性质,碱的化学性质
专题:元素化合物知识型
分析:A、盐酸和氯化钙的混合溶液的pH值小于7,而碳酸钠溶液的pH值大于7,可以据此解答该题;
B、向一定量的氢氧化钙溶液中通入二氧化碳,开始会生成碳酸钙,当氢氧化钙完全反应后,碳酸钙会与二氧化碳反应生成可溶性碳酸氢钙,可以据此解答该题;
C、酸的pH小于7,随着碳酸钠的加入,酸在不断消耗酸性减弱,直至反应完全pH等于7,再滴加碳酸钠溶液显碱性,pH大于7;
D、向盐酸和氯化铁的混合溶液中加氢氧化钠溶液,首先是碱与酸的反应,然后是氢氧化钠与氯化铁反应生成氢氧化铁的沉淀直至反应结束,可以据此解答该题.
B、向一定量的氢氧化钙溶液中通入二氧化碳,开始会生成碳酸钙,当氢氧化钙完全反应后,碳酸钙会与二氧化碳反应生成可溶性碳酸氢钙,可以据此解答该题;
C、酸的pH小于7,随着碳酸钠的加入,酸在不断消耗酸性减弱,直至反应完全pH等于7,再滴加碳酸钠溶液显碱性,pH大于7;
D、向盐酸和氯化铁的混合溶液中加氢氧化钠溶液,首先是碱与酸的反应,然后是氢氧化钠与氯化铁反应生成氢氧化铁的沉淀直至反应结束,可以据此解答该题.
解答:解:A、盐酸和氯化钙的混合溶液的pH值小于7,碳酸钠的pH值大于7,同时碳酸钠可以和盐酸、氯化钙反应,所以当向其中加入碳酸钠溶液时,因为碳酸钠和氯化钙反应生成的碳酸钙能够溶于稀盐酸,所以碳酸钠要先和盐酸反应,由于发生了反应而使溶液的pH值增大,直至它们恰好完全反应时,溶液的pH值为7,继续加入碳酸钠则碳酸钠由于和氯化钙反应生成了沉淀,溶液的pH值不变,直至氯化钙被完全反应掉;继续滴加碳酸钠溶液,则溶液的pH值要大于7,即乙图为向盐酸和氯化钙的混合溶液中滴加碳酸钠溶液,故A的图象和对应的操作相符;
B、向一定量的氢氧化钙溶液中通入二氧化碳,开始会生成碳酸钙,当氢氧化钙完全反应后,碳酸钙会与二氧化碳反应生成可溶性碳酸氢钙,所以沉淀是先多后少,最后为零.所以曲线应该是从零开始,慢慢增加到最大后慢慢回到零点,故B的图象和对应的操作相符;
C、酸的pH小于7,随着碳酸钠的加入酸在不断消耗酸性减弱,直至反应完全pH等于7,再滴加碳酸钠溶液显碱性,pH大于7,并逐渐变大,但不会无限制的增大,故C的图象和对应的操作不相符;
D、向盐酸和氯化铁的混合溶液中加氢氧化钠溶液,首先是碱与酸的反应,然后是氢氧化钠与氯化铁反应生成氢氧化铁的沉淀,直至反应结束,沉淀量不再改变,故D的图象和对应的操作相符;
故答案为:C.
B、向一定量的氢氧化钙溶液中通入二氧化碳,开始会生成碳酸钙,当氢氧化钙完全反应后,碳酸钙会与二氧化碳反应生成可溶性碳酸氢钙,所以沉淀是先多后少,最后为零.所以曲线应该是从零开始,慢慢增加到最大后慢慢回到零点,故B的图象和对应的操作相符;
C、酸的pH小于7,随着碳酸钠的加入酸在不断消耗酸性减弱,直至反应完全pH等于7,再滴加碳酸钠溶液显碱性,pH大于7,并逐渐变大,但不会无限制的增大,故C的图象和对应的操作不相符;
D、向盐酸和氯化铁的混合溶液中加氢氧化钠溶液,首先是碱与酸的反应,然后是氢氧化钠与氯化铁反应生成氢氧化铁的沉淀,直至反应结束,沉淀量不再改变,故D的图象和对应的操作相符;
故答案为:C.
点评:本题考查了常见物质的性质以及反应时的有关图象,解题的关键是要对每一个选项的变化过程有比较深入的了解,它对培养学生分析问题、识图判断能力的培养有一定帮助.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
如图所示是两种气体发生反应的微观示意图,其中相同颜色的球代表同种原子.下列说法正确的是( )


| A、原子在化学反应中可分 |
| B、化学反应前后原子的种类不变 |
| C、分子在化学变化中不可分 |
| D、反应后生成了两种新的物质 |
下列说法不正确的是( )
| A、化学变化的特征是放热,发光,变色,放出气体,生成沉淀 |
| B、汽车排气形成的烟雾是城市空气污染源之一 |
| C、工业上惰性气体常用作保护气,例如,电弧焊接铝合金时,可用氩气做保护气 |
| D、氮气和二氧化碳都是无色的,可用澄清石灰水区别二者 |
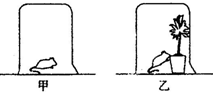 英国科学家普利斯特里曾做过一个实验.如图,在密闭玻璃容器甲内放一只小白鼠,在另一密闭玻璃容器乙内放一盆绿色植物和一只小白鼠,分别给予足够的光照,发现小白鼠在乙容器中比在甲容器中存活的时间长得多.此实验说明,植物在进行光合作用时会释放出
英国科学家普利斯特里曾做过一个实验.如图,在密闭玻璃容器甲内放一只小白鼠,在另一密闭玻璃容器乙内放一盆绿色植物和一只小白鼠,分别给予足够的光照,发现小白鼠在乙容器中比在甲容器中存活的时间长得多.此实验说明,植物在进行光合作用时会释放出