题目内容
葡萄糖(C6H12O6)经过发酵生成乙醇,可以用此方法来酿酒.(1)请完成该反应的化学方程式:C6H12O6
 2C2H5OH+______↑.
2C2H5OH+______↑.(2)已知水和乙醇的密度分别为1.0g/cm3和0.8g/cm3,将30体积乙醇和70体积的水混合,即成为30°的酒.则30°的酒中溶质的质量分数为______.
(3)若用某葡萄糖溶液经充分发酵得到30°的酒,试计算葡萄糖溶液中溶质的质量分数.
【答案】分析:(1)根据质量守恒定律的实质来完成化学方程式的书写;
(2)根据密度公式结合溶质的质量分数可以完成该题的解答;
(3)根据根据酒精的质量结合化学方程式求算出葡萄糖的质量,并根据溶质的质量分数来求算出溶液中溶质的质量分数.
解答:解:(1)比较反应前后元素的种类和原子的个数可以知道:反应后比反应前少了2个C,4个O,而该物质为气体,所以可以判断物质为CO2,其化学计量数为2,即该空应填:2CO2;
(2)30°的酒中溶质的质量分数为: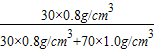 ×100%=25.5%
×100%=25.5%
(3)设葡萄糖溶液中溶质的质量为x,发酵后得到100g30°的酒.
C6H12O6 2C2H5OH+2CO2↑
2C2H5OH+2CO2↑
180 92
x 100g×25.5%=25.5g
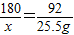
解得:x=49.89g
所以葡萄糖溶液中溶质的质量分数为: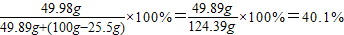
答:此葡萄糖溶液中溶质的质量分数约为40.1%.
故答案为:
(1)2CO2;
(2)25.5%;
(3)40.1%.
点评:本题主要考查学生运用化学方程式进行计算的能力,其中涉及到物理上的密度公式方面的知识,注意交叉学科知识的运用.
(2)根据密度公式结合溶质的质量分数可以完成该题的解答;
(3)根据根据酒精的质量结合化学方程式求算出葡萄糖的质量,并根据溶质的质量分数来求算出溶液中溶质的质量分数.
解答:解:(1)比较反应前后元素的种类和原子的个数可以知道:反应后比反应前少了2个C,4个O,而该物质为气体,所以可以判断物质为CO2,其化学计量数为2,即该空应填:2CO2;
(2)30°的酒中溶质的质量分数为:
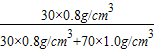 ×100%=25.5%
×100%=25.5%(3)设葡萄糖溶液中溶质的质量为x,发酵后得到100g30°的酒.
C6H12O6
 2C2H5OH+2CO2↑
2C2H5OH+2CO2↑180 92
x 100g×25.5%=25.5g
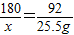
解得:x=49.89g
所以葡萄糖溶液中溶质的质量分数为:
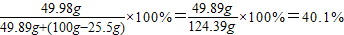
答:此葡萄糖溶液中溶质的质量分数约为40.1%.
故答案为:
(1)2CO2;
(2)25.5%;
(3)40.1%.
点评:本题主要考查学生运用化学方程式进行计算的能力,其中涉及到物理上的密度公式方面的知识,注意交叉学科知识的运用.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
