题目内容
12.(1)NH4NO3中,氮、氢、氧原子个数比为2:4:3(2)硝酸铵中氮、氢、氧元素的质量比7:1:12.
(3)求100克NH4NO3中氮元素的质量.
分析 (1)根据硝酸铵的化学式可以求出硝酸铵中氮氢氧原子个数比;
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数═$\frac{该元素的相对原子质量\;\;×\;\;\;原子个数\;\;\;\;\;}{化合物的相对分子质量}$×100%,然后求出硝酸铵这氮元素的质量即可.
解答 解:(1)1个硝酸铵分子是由2个氮原子、4个氢原子和3个氧原子构成的,则硝酸铵分子中氮、氢、氧的原子个数比为2:4:3.故填:2:4:3;
(2)硝酸铵中氮、氢、氧三种元素的质量之比是(14×2):(1×4):(16×3)=7:1:12.故填:N:H:O=7:1:12;
(3)100g硝酸铵中含有氮元素的质量为:100g×$\frac{14×2}{14+1×4+14+16×3}×100%$=35g
答:100g硝酸铵中含有氮元素的质量为35g.
故答案为:(1)2:4:3;(2)7:1:12;(3)35g.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
4.下列对分子、原子、离子的认识正确的是( )
| A. | 温度越高,分子运动速率越快 | |
| B. | 原子是最小的粒子,不可再分 | |
| C. | 离子不能直接构成物质 | |
| D. | 固体难压缩,说明固体分子间无间隔 |
1.实验室制取氧气的主要操作有以下几步:
①熄灭酒精灯;
②使用排水法收集氧气;
③将装有氯酸钾和二氧化锰混合物的试管用带有导管的橡皮胶塞塞紧,并固定在铁架台上;
④点燃酒精灯,对试管进行加热;
⑤检查装置的气密性;
⑥实验完毕,把导管从水槽中取出.
操作正确顺序是( )
①熄灭酒精灯;
②使用排水法收集氧气;
③将装有氯酸钾和二氧化锰混合物的试管用带有导管的橡皮胶塞塞紧,并固定在铁架台上;
④点燃酒精灯,对试管进行加热;
⑤检查装置的气密性;
⑥实验完毕,把导管从水槽中取出.
操作正确顺序是( )
| A. | ⑤③④②⑥① | B. | ⑤③④②①⑥ | C. | ③⑤②④①⑥ | D. | ⑤②③④⑥① |
2.下列关于氧气的说法正确的是( )
| A. | 氧气易溶于水 | |
| B. | 氧气有可燃性 | |
| C. | 食物腐败不需要氧气 | |
| D. | 在压强为101kPa时,氧气在-183℃时变为淡蓝色液体 |

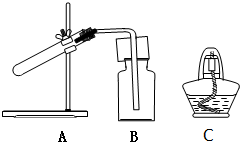 在实验室中,利用如图装置可以制取并收集多种气体(必要时可以加热)
在实验室中,利用如图装置可以制取并收集多种气体(必要时可以加热)