题目内容
19.用双氧水制取氧气时,加了催化剂,其结果是( )| A. | 放出氧气的总量不变、速率会变快 | B. | 放出氧气的总量会增加、速率变快 | ||
| C. | 放出氧气的总量和速率不受影响 | D. | 放出氧气的总量会减少 |
分析 在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫做催化剂(又叫触媒).催化剂的特点可以概括为“一变二不变”,一变是能够改变化学反应速率,二不变是指质量和化学性质在化学反应前后保持不变.
解答 解:催化剂只能改变化学反应速率,但对生成物的质量无影响,使用催化剂不能增加生成物的质量.
A、用双氧水制取氧气时,加了催化剂,放出氧气的总量不变,放出氧气的速率会变快,故选项说法正确.
B、用双氧水制取氧气时,加了催化剂,放出氧气的总量不变,故选项说法错误.
C、用双氧水制取氧气时,加了催化剂,放出氧气的总量不变,放出氧气的速率会变快,故选项说法错误.
D、用双氧水制取氧气时,加了催化剂,放出氧气的总量不变,故选项说法错误.
故选:A.
点评 本题难度不大,考查对催化剂概念的理解,掌握催化剂的特征(“一变二不变”)是正确解答本题的关键

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7. 实验室制取氧气的装置如图所示,下列有关叙述合理的是( )
实验室制取氧气的装置如图所示,下列有关叙述合理的是( )
 实验室制取氧气的装置如图所示,下列有关叙述合理的是( )
实验室制取氧气的装置如图所示,下列有关叙述合理的是( )| A. | 锥形瓶里加入少量MnO2粉末,分液漏斗里盛放6%双氧水 | |
| B. | 锥形瓶里加入高锰酸钾固体,分液漏斗里盛放蒸馏水 | |
| C. | 该装置的优点是能控制反应的发生和停止 | |
| D. | 当发生装置中液体与固体一接触产生了气泡即刻收集 |
9.小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是他对氧化铜产生了探究兴趣.
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
查阅资料:氯酸钾、氯化钾等固体可以溶解于水,二氧化锰、氧化铜等固体不溶于水.
【设计实验】小雨以生成100毫升的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略).
(1)上述实验应测量的“待测数据”是收集100毫升的氧气所用的时间;
(2)若实验②比实验①的“待测数据”更小(填“大”或“小”),说明 氧化铜能加快氯酸钾的分解速率.
(3)将实验②反应后的固体进行加水溶解、过滤(填操作名称)、洗涤干燥、称量等步骤后,得到黑色粉末0.5g.
(4)将步骤(3)得到的黑色粉末放入另一试管中,向试管中倒入适量的双氧水(重复多次此实验),观察到试管中均能迅速产生大量气泡.
试写出该反应的符号表达式H2O2$\stackrel{CuO}{→}$H2O+O2↑.
【预期结论】综合以上步骤(2)(3)(4)可得出氧化铜能作氯酸钾的催化剂.
【评价设计】你认为小雨设计实验③和实验②对比的目的是对比氧化铜和二氧化锰的催化效果.
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
查阅资料:氯酸钾、氯化钾等固体可以溶解于水,二氧化锰、氧化铜等固体不溶于水.
【设计实验】小雨以生成100毫升的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略).
| 实验序号 | 氯酸钾质量 | 其它物质质量 | 待测数据 |
| ① | 1.5g | ||
| ② | 1.5g | CuO 0.5g | |
| ③ | 1.5g | MnO2 0.5g |
(2)若实验②比实验①的“待测数据”更小(填“大”或“小”),说明 氧化铜能加快氯酸钾的分解速率.
(3)将实验②反应后的固体进行加水溶解、过滤(填操作名称)、洗涤干燥、称量等步骤后,得到黑色粉末0.5g.
(4)将步骤(3)得到的黑色粉末放入另一试管中,向试管中倒入适量的双氧水(重复多次此实验),观察到试管中均能迅速产生大量气泡.
试写出该反应的符号表达式H2O2$\stackrel{CuO}{→}$H2O+O2↑.
【预期结论】综合以上步骤(2)(3)(4)可得出氧化铜能作氯酸钾的催化剂.
【评价设计】你认为小雨设计实验③和实验②对比的目的是对比氧化铜和二氧化锰的催化效果.
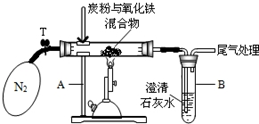 某学生小组对过量碳粉与氧化铁反应产物中气体的成分进行研究.
某学生小组对过量碳粉与氧化铁反应产物中气体的成分进行研究.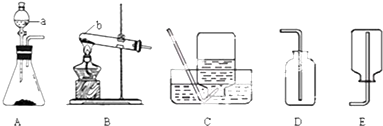
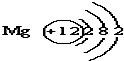 已知镁元素的原子结构示意图如图.请回答:
已知镁元素的原子结构示意图如图.请回答: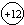 表示的意义核内有12个质子;
表示的意义核内有12个质子;