题目内容
17.科学兴趣小组做了如下实验:将一镁条放入CuCl2溶液中,镁条表面覆盖了红色物质,但很快镁条表面又冒出很多气泡,他们觉得很奇怪.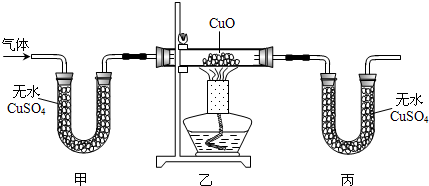
【提出问题】这些气泡究竟是怎样产生的?是什么气体呢?
【猜想】小科:是氧气;小丽:是氯化氢;小琪:是氨气(NH3);小梁:是氢气.小黄马上否定了小琪的猜想,他否定的依据是质量守恒定律(或反应物中没有氮元素);
【实验探究】他们开始着手收集所产生的气体.
实验一:小科用带火星的木条检验该气体,木条不复燃.说明生成的气体不是氧气;
实验二:为继续探究反应后生成的气体是否是氯化氢,小丽用湿润的蓝色石蕊试纸检验该气体,试纸不变红,说明生成的气体不是氯化氢;
实验三:为确定气体是否是氢气,小梁设计了如图的实验装置(每个装置的反应均完全).
【实验结论】(1)若该气体是氢气,则在乙装置中可以观察到的现象是黑色粉末变红.
(2)甲、丙装置中无水硫酸铜的作用是不同的,请指出它们的区别甲是除去原气体中的水蒸气,丙是验证有水生成.
(3)为确定该气体产生的本质原因,小梁用精密pH试纸测试实验所用的CuCl2溶液,pH约为5.5,最后确定CuCl2溶液呈酸性.查阅资料发现:CuCl2为强酸弱碱盐,其水溶液酸碱性与实验结果相符.
分析 【猜想】根据反应物是镁和CuCl2溶液分析判断;
【实验结论】(1)根据氢气具有还原性分析;
(2)检验气体的成分,首先除去水分的干扰;无水硫酸铜可以检验水分的存在.
解答 解:【猜想】反应物是镁和CuCl2溶液,没有N元素,根据质量守恒定律可知,小琪的猜想不对;
【实验探究】酸性溶液使蓝色石蕊试纸变红.氯化氢是酸性气体,小丽用湿润的蓝色石蕊试纸检验该气体,试纸不变红,说明生成的气体不是氯化氢;
【实验结论】(1)氢气具有还原性,能够还原氧化铜,生成红色铜.所以若该气体是氢气,则在乙装置中可以观察到的现象是黑色粉末变红;
(2)检验气体的成分,首先除去水分的干扰,无水硫酸铜能够吸收水分,所以甲中的无水硫酸铜是除去原气体中的水蒸气;无水硫酸铜遇水变蓝,所以无水硫酸铜可以检验水分的存在,丙中的无水硫酸铜是验证有水生成.
故答案为:【猜想】质量守恒定律(或反应物中没有氮元素);
【实验结论】(1)黑色粉末变红;
(2)甲是除去原气体中的水蒸气,丙是验证有水生成.
点评 通过实验考查物质的性质,训练同学们的实验探究能力,难度不大.

练习册系列答案
相关题目
20.请选出按混合物、氧化物、单质的顺序排列的一组物质( )
| A. | 食盐水、水、液态氧 | B. | 水银、二氧化氮、氮气 | ||
| C. | 洁净的空气、过氧化氢、氯化钠 | D. | 大理石、高锰酸钾、干冰 |
5.如图是氢氧化钙的溶解度曲线.在酉阳的冬天气温为5℃时配制的氢氧化钙饱和溶液,在夏天气温为36℃时(水的蒸发忽略不计),不可能出现的情况是( )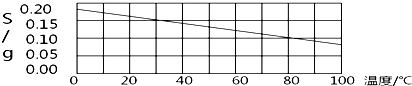

| A. | 溶液变为不饱和 | B. | 氢氧化钙的溶解能力降低 | ||
| C. | 溶液质量变小 | D. | 溶质质量分数变小 |
12.下列各组物质的稀溶液,不用其他试剂就能鉴别出来的是( )
| A. | Na2CO3、HCl、CaCl2、HNO3 | B. | FeCl3、NaOH、Na2SO4、KCl | ||
| C. | KNO3、HCl、NaOH、FeCl3 | D. | NH4Cl、KOH、Na2SO4、BaCl2 |
2.在下列变化中,既不属于化合反应,也不属于分解反应而是属于氧化反应的是( )
| A. | 木炭+氧气$\stackrel{点燃}{→}$二氧化碳 | B. | 石蜡+氧气$\stackrel{点燃}{→}$二氧化碳+水 | ||
| C. | 氧化汞$\stackrel{加热}{→}$汞+氧气 | D. | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁 |
7.不同种元素的本质区别是( )不同.
| A. | 中子数 | B. | 质子数 | C. | 核外电子数 | D. | 相对原子质量 |