题目内容
3.现有如图所示的实验装置: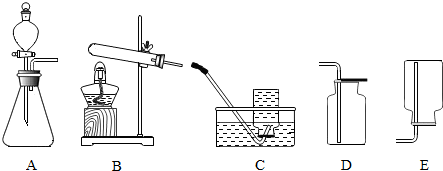
(1)A装置可用于制二氧化碳的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O.该发生装置还可以用来制取其它气体,写反应的化学方程式:Zn+H2SO4═ZnSO4+H2↑(或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑).
(2)用D装置收集二氧化碳气体时,如何验满:将燃着的木条放于集气瓶口,若木条熄灭则满.
(3)实验室中常用加热氯化铵与熟石灰的固体混合物的方法来制取氨气.制氨气的发生装置应选用B(填字母)装置;收集氨气只能选用E装置,由此推断氨气具有的物理性质是密度比空气小,易溶于水.
分析 (1)A装置属于固液常温制取气体,并结合实验室制取氧气、氢气、二氧化碳的方法分析解答;
(2)验满二氧化碳的方法是:将燃着的木条放于集气瓶口,观察木条是否熄灭进行判断;
(3)据反应物状态和反应条件选择发生装置,只能用向下排空气法收集,说明氨气密度比空气小,易溶于水.
解答 解:(1)实验室制取二氧化碳用大理石和稀盐酸反应,反应方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;氢气、氧气实验室制法的反应原理Zn+H2SO4═ZnSO4+H2↑,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,都是固体和液体的反应,都可用“固液混合不加热”型气体发生装置,即A装置来制取;
(2)验满二氧化碳的方法是:将燃着的木条放于集气瓶口,观察木条是否熄灭进行判断;
(3)用加热氯化铵与熟石灰的固体混合物的方法来制取氨气,属于固体加热型,故选发生装置B,只能用向下排空气法收集,说明氨气密度比空气小,易溶于水;
故答案为:(1)CaCO3+2HCl=CaCl2+CO2↑+H2O;Zn+H2SO4═ZnSO4+H2↑(或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑);
(2)将燃着的木条放于集气瓶口,若木条熄灭则满;
(3)B;密度比空气小,易溶于水.
点评 本题主要考查常见气体的发生装置与收集装置的探究,以及反应原理和气体的验满,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
相关题目
11.广东盛产荔枝,其部分营养成分如右表.请回答:
(1)荔枝中含有能提供能量的营养素有3种.
(2)每200g荔枝中含含有大量的维生素C82.00ug,若人体缺乏维生素C会患坏血病.
| 荔枝的部分营养成分(100克中含) |
| 糖类16.60g 蛋白质0.90g 脂肪0.20g 维生素A 2.00ug 维生素C 41.00ug 钙 2.00mg 鉀 151.00mg 铁 0.40mg 硒 0.14ug… |
(2)每200g荔枝中含含有大量的维生素C82.00ug,若人体缺乏维生素C会患坏血病.
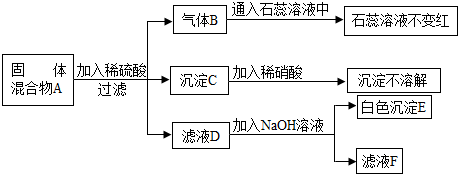
8. 下列是初中常见物质,由下表中元素组成.
下列是初中常见物质,由下表中元素组成.
(1)A溶于水形成黄色溶液,其化学式为FeCl3.
(2)B是由三种元素组成的有机物,是化学实验室的常用燃料,写出该物质燃烧的化学方程式C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
(3)C和D是常用的灭火剂,D与E反应能生成C,写出D与E反应的化学方程式CO2+2NaOH=Na2CO3+H2O.
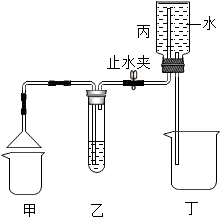
(4)用如图装置进行实验时,打开止水夹,丙中水流入丁中,乙中有气泡冒出.若甲中盛有溶液F,乙中盛有含酚酞的E溶液,实验时观察到乙中溶液变为无色.充分反应后乙中溶质(不包含酚酞)的可能组成为酚酞、NaCl;或酚酞、NaCl、HCl.
 下列是初中常见物质,由下表中元素组成.
下列是初中常见物质,由下表中元素组成.| 元素名称 | 氢 | 碳 | 氧 | 氯 | 钠 | 铁 |
| 元素符号 | H | C | O | Cl | Na | Fe |
(2)B是由三种元素组成的有机物,是化学实验室的常用燃料,写出该物质燃烧的化学方程式C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
(3)C和D是常用的灭火剂,D与E反应能生成C,写出D与E反应的化学方程式CO2+2NaOH=Na2CO3+H2O.
(4)用如图装置进行实验时,打开止水夹,丙中水流入丁中,乙中有气泡冒出.若甲中盛有溶液F,乙中盛有含酚酞的E溶液,实验时观察到乙中溶液变为无色.充分反应后乙中溶质(不包含酚酞)的可能组成为酚酞、NaCl;或酚酞、NaCl、HCl.
15.小雨将日常生活中一些化学信息归纳成有趣的“三要点”,下列说法中有错误的是( )
| A. | 去油污的方法有三种:用汽油擦洗、用洗涤剂清洗、用热的碳酸钠溶液洗涤 | |
| B. | 人体主要提供热能的营养素有三种:蛋白质、维生素、糖类 | |
| C. | 我国古代流传至今的三大杰出化学工艺:造纸、制火药、烧瓷器 | |
| D. | 氢能源广泛推广有三大障碍:制取成本高、易泄漏贮存难、不安全 |
2.市售的“脑黄金”(DHA)是从深海鱼油中提取的,其主要成分的化学式为C25H51COOH,下列关于“脑黄金”的说法中正确的是( )
| A. | 它是一种氧化物 | |
| B. | 它是由C25H51COOH 分子构成 | |
| C. | 它是由26个碳元素、52个氢元素和2个氧元素组成的 | |
| D. | 脑黄金中碳、氢、氧三种元素的质量比26:52:2 |