题目内容
19.在一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后个物质的质量如表所示.根据表中信息判断下列说法正确的是( )| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量/g | 2 | 30 | 20 | 10 |
| 反应后的质量/g | m | 39 | 5 | 16 |
| A. | 该反应是化合反应 | |
| B. | 甲是该反应的催化剂 | |
| C. | 反应过程中乙、丙变化的质量比为3:5 | |
| D. | 丙可能是单质 |
分析 利用反应物质量会减小生成物质量会增加,催化剂质量不变,以及反应类型的特点解决.
解答 解:反应前物质的总质量为:2g+30g+20g+10g=62g,反应后物质的总质量为:m+39+5+16=62,则m=2,甲质量没变,可是该反应的催化剂;乙丁质量增加,应为该反应的生成物;丙质量减少,应为该反应的反应物;
A、由以上分析,丙生成乙和丁,故反应为分解反应,故A错误;
B、甲反应前后质量没变,故可能为催化剂,也可能不参加反应,故B说法错误;
C、乙增加了39g-30g=9g,丙减少了20g-5g=15g,故乙、丙变化的质量比为9g:15g=3:5,故C说法正确;
D、丙是分解反应的反应物,是化合物,故D说法错误;
故选C.
点评 本题主要考查质量守恒定律的应用、反应物和生成物的判断、基本反应类型的判断等,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列各微粒结构示意图中,能表示阳离子的是( )
| A. | 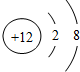 | B. | 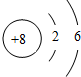 | C. | 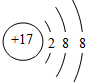 | D. | 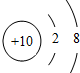 |
7.取铜和氧化铜的混合物10g,用足量的一氧化碳还原后共得到8.4g固体物质,则原混合物中含氧化铜的质量分数为( )
| A. | 80% | B. | 100% | C. | 78% | D. | 84% |
14.下列物质由离子构成的是( )
| A. | 水 | B. | 氮气 | C. | 氯化钠 | D. | 二氧化碳 |
8.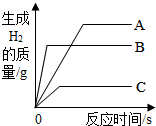 将质量相等的A、B、C三种金属(均为+2价),同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是( )
将质量相等的A、B、C三种金属(均为+2价),同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是( )
 将质量相等的A、B、C三种金属(均为+2价),同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是( )
将质量相等的A、B、C三种金属(均为+2价),同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是( )| A. | 放出H2的质量是A>B>C | B. | 金属活动性顺序是A>B>C | ||
| C. | 反应速率最大的是A | D. | 相对原子质量是C<B<A |
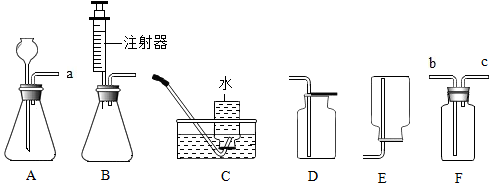
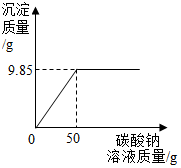 小红同学在某化工厂进行社会实践,技术员与小红一起分析由氯化钡和氯化钠组成的产品中氯化钠的质量分数.取16.25g固体样品,全部溶于143.6g水中,向所得到的混合溶液中逐滴加入溶质质量分数为10.6%的碳酸钠溶液,记录了如图所示的曲线关系.技术员给小红的提示:反应的化学方程式BaCl2+Na2CO3═BaCO3↓+2NaCl
小红同学在某化工厂进行社会实践,技术员与小红一起分析由氯化钡和氯化钠组成的产品中氯化钠的质量分数.取16.25g固体样品,全部溶于143.6g水中,向所得到的混合溶液中逐滴加入溶质质量分数为10.6%的碳酸钠溶液,记录了如图所示的曲线关系.技术员给小红的提示:反应的化学方程式BaCl2+Na2CO3═BaCO3↓+2NaCl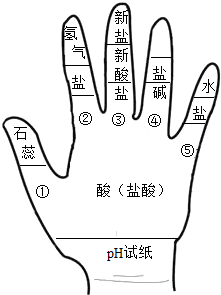 构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题: