题目内容
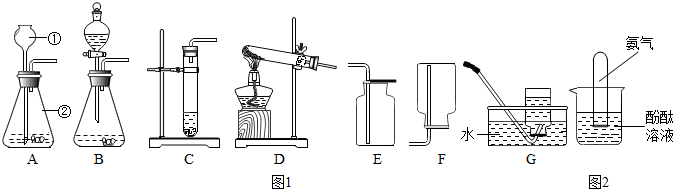
14.请结合下图实验常用装置,回答有关问题.
(1)写出图中标有字母的仪器名称:a长颈漏斗.
(2)若用高锰酸钾制取氧气,应选用的发生装置是A(填“A”、“B”或“C”),在加入药品前,应首先检查装置气密性,加药品后试管口还应放置一团棉花,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MO2+O2↑.
(3)若要制取二氧化碳,在B装置中装有石灰石,那么a中应加入稀盐酸 (填写试剂名称),反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑,如果用E装置收集该气体,则气体从b端进入(填“b”或“c”).
(4)实验室如用块状固体和液体无需加热制取难溶性气体,可将B装置改进为C装置(多孔隔板用来放块状固体),其最突出的优点是随时控制反应的发生与停止.
(5)实验室常用氯化铵晶体跟氢氧化钙粉末混合加热制取氨气.它是一种无色、有刺激性气味、密度比空气小、易溶于水的气体,制取氨气过程中还有氯化钙和水生成.
①写出制取氨气反应的文字表达式:氢氧化钙+氯化铵$\stackrel{加热}{→}$氨气+水+氯化钙;
②实验室制取氨气的发生装置,可选用制取A (填“A”或“B”)的装置.其理由是反应物是固体且反应需要加热;收集氨气可用向下排空气法,理由是氨气密度比空气小.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,在加入药品前,应首先检查装置气密性,加药品后试管口还应放置一团棉花,防止高锰酸钾粉末进入导管,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
(3)根据要制取二氧化碳,在B装置中装有石灰石,那么a中应加入稀盐酸,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,二氧化碳密度比空气大进行分析;
(4)根据C装置制取气体的发生装置中隔板及活塞的作用分析优点;
(5)①根据氢氧化钙和氯化铵在加热的条件下生成氯化钙、水和氨气进行分析;
②根据实验室制取氨气的反应物是固体,反应条件是加热,氨气密度比空气小、易溶于水进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是长颈漏斗;
(2)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,所以应选用的发生装置是A,在加入药品前,应首先检查装置气密性,加药品后试管口还应放置一团棉花,防止高锰酸钾粉末进入导管,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MO2+O2↑;
(3)要制取二氧化碳,在B装置中装有石灰石,那么a中应加入稀盐酸,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑,二氧化碳密度比空气大,所以用E装置收集该气体,则气体从b端进入;
(4)B装置使用分液漏斗的优点是通过控制过氧化氢溶液的滴加速度,从而控制反应的速率;C装置使用隔板放置固体,可以通过活塞控制装置内的气压使固液接触或分离,因此可以随时控制反应的发生和停止;
(5)①氢氧化钙和氯化铵在加热的条件下生成氯化钙、水和氨气,文字表达式为:氢氧化钙+氯化铵$\stackrel{加热}{→}$氨气+水+氯化钙;
②实验室制取氨气的反应物是固体,反应条件是加热,所以发生装置可选用A,氨气密度比空气小、易溶于水,收集氨气可用向下排空气法.
故答案为:(1)长颈漏斗;
(2)A,检查装置气密性,棉花,2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MO2+O2↑;
(3)稀盐酸,CaCO3+2HCl═CaCl2+H2O+CO2↑,b;
(4)随时控制反应的发生与停止;
(5)①氢氧化钙+氯化铵$\stackrel{加热}{→}$氨气+水+氯化钙;
②A,反应物是固体且反应需要加热,向下排空气法,氨气密度比空气小.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 金钥匙试卷系列答案
金钥匙试卷系列答案| A. | Ag2O | B. | CuSO4 | C. | H2 | D. | NaCl |
①试管 ②集气瓶 ③蒸发皿 ④量筒 ⑤烧杯 ⑥燃烧匙 ⑦石棉网.
| A. | ①③④⑥ | B. | ①②⑤⑦ | C. | ①③⑥⑦ | D. | ②③⑤⑥ |

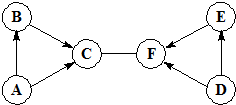 A、B、C、D、E、F是初中化学上册常见的六种物质,它们之间有如图所示的关系,箭头表示一种物质可以转化成另一种物质,C和F能反应.其中A、B、C含有一种相同的元素,D、E、F含有另一种相同的元素.
A、B、C、D、E、F是初中化学上册常见的六种物质,它们之间有如图所示的关系,箭头表示一种物质可以转化成另一种物质,C和F能反应.其中A、B、C含有一种相同的元素,D、E、F含有另一种相同的元素.