题目内容
16.整理和归纳是有效的学习方法.下面是某学习小组的同学对Mg、Fe、Cu、Hg、Ag五种金属相关知识的归纳复习,请你参与并回答问题:(1)从物理性质上看,常温下为液态的金属是Hg.
(2)从化学性质上看,与盐酸反应最剧烈的是Mg,这五种金属中,有一种金属的盐溶液能与其他四种金属发生反应,该金属是Ag.
(3)性质决定用途,用途反映性质是重要的化学学科思想.用镁粉制作的烟花在夜空中发出耀眼的白光,这是利用了镁的可燃性,燃烧产物为氧化镁.
分析 汞在常温下为液态的金属,而其他金属都是固态,在金属活动性顺序中,氢前的金属能与酸发生置换反应,位置越靠前,反应的越剧烈,位置在前的金属能把位于其后的金属从其盐溶液中置换出来.
解答 解:(1)分析所给的五种金属,汞在常温下为液态的金属,而其他金属都是固态,所以本题答案为:Hg;
(2)在金属活动性顺序中,镁和铁在氢的前面,且镁在铁的前面,故镁是最活泼的金属,所以与盐酸反应最剧烈,有一种金属的盐溶液能与其他四种金属发生反应,说明该金属活动性最弱,该金属为银,所以本题答案为:Mg,Ag;
(3)镁燃烧时能发出耀眼的白光,生成白色的氧化镁,可以用于制作烟花,所以本题答案为:可燃;氧化镁.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
6.下边为甲(  )与乙(
)与乙(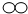 )反应生成丙(
)反应生成丙( )的粒子数变化示意图,
)的粒子数变化示意图,
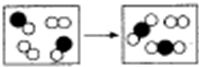
则下列说法正确的是( )
 )与乙(
)与乙( )反应生成丙(
)反应生成丙( )的粒子数变化示意图,
)的粒子数变化示意图,
则下列说法正确的是( )
| A. | 甲一定是氧化物 | B. | 如图的物质是纯净物 | ||
| C. | 该反应类型是分解反应 | D. | 该反应类型是化合反应 |
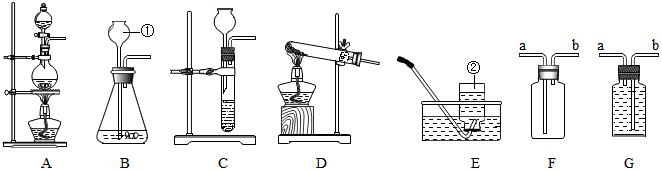
4.下列实验操作错误的是( )
| A. |  | B. | 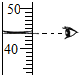 | C. |  | D. |  |
1.学习常见金属的化学性质和金属的活动性顺序,能帮助我们发现和研究更多的金属.
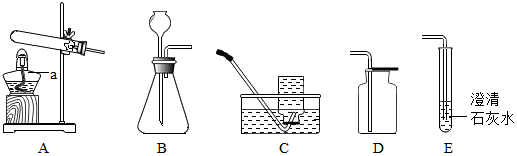
(1)根据如图回答有关问题:

①写出实验A中反应的主要实验现象剧烈燃烧,火星四射,放热,生成黑色固体
写出实验B中反应的化学方程式:Fe+CuSO4=FeSO4+Cu
②实验B中可观察到铁片的表面覆盖一层红色物质现象,说明铁的金属活动性比铜强.(填“强”或“弱”)
③实验C中可观察到试管中铁钉最先生锈的是b处.(填“a”或“b”或“c”)
(2)所谓合金,就是不同种金属(或金属与非金属)在熔化状态下形成的一种熔合物.
根据上表中四种金属的熔沸点,判断其中不能形成合金的是c.
a.Cu和Al b.Fe和Cu c.Fe和Na
(3)某兴趣小组的同学在实验室为了比较银白色金属R与铁的活动性强弱,设计了下列方案进行实验,请你帮他们完成下表:
(1)根据如图回答有关问题:

①写出实验A中反应的主要实验现象剧烈燃烧,火星四射,放热,生成黑色固体
写出实验B中反应的化学方程式:Fe+CuSO4=FeSO4+Cu
②实验B中可观察到铁片的表面覆盖一层红色物质现象,说明铁的金属活动性比铜强.(填“强”或“弱”)
③实验C中可观察到试管中铁钉最先生锈的是b处.(填“a”或“b”或“c”)
(2)所谓合金,就是不同种金属(或金属与非金属)在熔化状态下形成的一种熔合物.
| Na | Cu | Al | Fe | |
| 熔点(℃) | 97.5 | 1083 | 660 | 1535 |
| 沸点(℃) | 883 | 2595 | 2200 | 3000 |
a.Cu和Al b.Fe和Cu c.Fe和Na
(3)某兴趣小组的同学在实验室为了比较银白色金属R与铁的活动性强弱,设计了下列方案进行实验,请你帮他们完成下表:
| 你的一种猜想 | 验证方法 | 现象 | 结论 |
| 金属R活动性比铁强 | 将金属R投入 硫酸亚铁溶液中 | 金属R表面有黑色的物质析出 | 猜想正确 (选填“正确”或“错误”) |
5.在某化学反应 2XY+Y2═2Z中,Z物质的化学式符合( )
| A. | X2Y2 | B. | X2Y | C. | XY2 | D. | X3Y2 |
6.学习化学常常要做实验,下列操作正确的是( )
| A. | 将鼻子凑到容器口去闻药品的气味 | B. | 用过滤法除去水中的难溶性杂质 | ||
| C. | 直接用手拿药品 | D. | 将用剩的药品直接倒回原瓶中 |