题目内容
(6分)取碳酸钠和氯化钠的混合物10g,投入50g溶质质量分数为9.8%的稀硫酸中,恰好完全反应,假设生成的气体全部逸出。计算:
(1)反应中生成二氧化碳气体的质量;
(2)该混合物中碳酸钠的质量分数。

(提示:反应的化学方程式为Na2CO3+
H2SO4  Na2SO4
+ H2O + CO2↑)
Na2SO4
+ H2O + CO2↑)
【答案】
设反应中生成二氧化碳气体的质量为 ,样品中的碳酸钠的质量为
,样品中的碳酸钠的质量为 。
。
Na2CO3+H2SO4=Na2SO4+H2O +CO2↑
106 98 44
 50g×98%
50g×98%


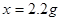



答:生成二氧化碳气体的质量为2.2g,样品中碳酸钠的质量分数为53%。
【解析】略

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目







