题目内容
氯化铁是一种重要的铁盐,广泛用于造纸、印染等污染处理。
【物质制备】某兴趣小组同学查找到以黄铁矿(主要成分是二硫化亚铁,化学式为FeS2)为主要原料制备氯化铁晶体的工业生产过程:
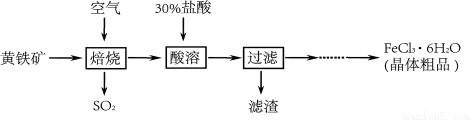
(1)黄铁矿是 物(填“纯净”或“混合”),其中二硫化亚铁中铁元素的化合价为 。
(2)焙烧过程主要发生以下化学反应,配平化学方程式: FeS2 + O2 高温Fe2O3 + SO2
(3)该过程产生的尾气中含有HCl等气体,可用 溶液来吸收(填化学式)。
【含量测定】在上述流程中产生的SO2气体可用于工业上生产硫酸,该兴趣小组的同学为测定某黄铁矿中硫元素的含量进行了如下的实验探究。
已知二氧化硫与氢氧化钠反应生成的亚硫酸钠能被过氧化氢氧化成硫酸钠。(假设每步反应均完全,不考虑装置内原有空气对测定结果的影响)
甲、乙二个实验小组均设计了下列装置,称取了m1 g黄铁矿样品,将样品放入如下图所示的硬质粗玻璃管中,从a处不断地缓缓通入空气,高温灼烧玻璃管中的黄铁矿样品至反应完全。
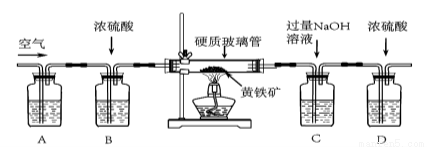
甲组同学仅称量了上述实验所需要的相关装置质量后即完成了测定。
乙组同学则在上述反应结束后,将C瓶中的溶液进行了如下图处理:

问题讨论:
(4)上述装置中A瓶内所盛的试剂最好是 溶液,其作用是 。
A、B装置能否对调位置? (填“能”或“否”)
(5)气体进入C瓶后,C瓶中发生反应的化学方程式为 。
(6)甲组同学应称量的数据是 (填编号)。
①反应前C装置及其中物质总质量m2 g
②反应前C、D装置及其中物质总质量m3 g
③反应后C装置及其中物质总质量m4 g
④反应后C、D装置及其中物质总质量m5 g
(7)根据(6)中所选数据,甲组同学测得的该黄铁矿中硫元素的质量分数的表达式为 。
(8)乙组同学最终得到的固体的化学式为 ,检验所加BaCl2溶液是否过量的方法是 ,乙组的实验过程中洗涤滤渣的目的是 ,若未洗涤就直接烘干称量,则会使测定结果 (填“偏大、偏小或不变”),检验滤渣是否洗净所用试剂是 溶液,该小组测定的硫元素的质量分数的表达式为 。
(1)混合 +2
(2)4 11 2 8 (共1分)
(3)NaOH等
(4)NaOH 吸收空气中的CO2 否
(5)SO2 + 2 NaOH = Na2SO3 + H2O
(6)②④
(7)(m5-m3)/2m1
(8)BaSO4 静置,在上层清液再加BaCl2溶液,若无沉淀产生,则已过量
除去沉淀表面的可溶性杂质 偏大 AgNO3 /碳酸钠/硫酸钠等 ; 32 m6/233 m1
【解析】
试题分析:(1)黄铁矿是混合物,根据化合物中各元素正负化合价代数和为0,可知铁的化合价为+2;(2)根据化学反应前后各原子种类和原子个数不变进行配平。(3)HCl为酸性气体,可用碱溶液来吸收(4)氢氧化钠溶液能与空气中的二氧化碳反生反应,AB不能互换,互换后不能除去空气中的二氧化碳和水,会对后边的实验造成干扰;(5)二氧化硫和氢氧化钠反应,生成亚硫酸钠和水;(6)C、D装置中增加的质量是反应后生成的二氧化硫的质量,知道了二氧化硫的质量,再结合样品的质量即可计算出硫元素质量分数,故选②④ ;(7)二氧化硫中硫元素质量分数为50%,所以根据(6)中所选数据可计算出样品中硫元素质量分数。(8)过氧化氢具有很强的氧化性,将亚硫酸钠氧化呈硫酸钠,硫酸钠和氯化钡生成硫酸钡沉淀,所以乙组同学最终得到的固体为硫酸钡;检验所加氯化钡是否过量的方法是取上层清液再加氯化钡,若有白色沉淀,则证明已经过量;乙组的实验过程中洗涤滤渣的目的是除去沉淀表面的可溶性杂质,若未洗涤,直接烘干称量,会使结果偏大,检验滤渣是否洗净所用试剂是硝酸银溶液或碳酸钠溶液等;根据质量守恒可以计算出硫铁矿中硫的质量,从而得出硫元素的质量分数为32 m6/233 m1
考点:物质间的相互转化,质量守恒定律的应用,化学用语。

 阅读快车系列答案
阅读快车系列答案对下列事实的微观解释错误的是
选项 | 事 实 | 解 释 |
A | 一氧化碳有毒而二氧化碳无毒 | 两种物质的分子构成不同 |
B | 品红在热水中扩散速度更快 | 受热情况下,分子运动速率加快 |
C | 盐酸、稀硫酸都能使紫色石蕊溶液变红 | 两种溶液中都含有氢离子 |
D | 温度计中的酒精受热膨胀 | 原子间的间隔受热时增大 |
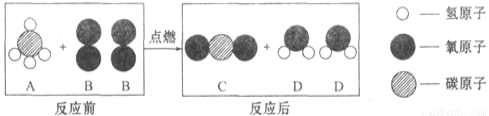
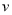 (CH4):
(CH4):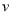 (O2)等于5:2
(O2)等于5:2 CO2 + 2H2O
CO2 + 2H2O