题目内容
8.往盐酸溶液里加入一定量的氢氧化钠溶液,无任何明显现象.以下实验操作一定可证明二者确实发生了反应的是( )| A. | 测量混合前后溶液的pH值,发现混合后溶液的pH值升高了 | |
| B. | 往反应后溶液中加入酚酞,发现酚酞变红 | |
| C. | 往反应后溶液中滴加硝酸银溶液,出现了白色沉淀 | |
| D. | 往反应后溶液中加入金属锌,无任何现象 |
分析 盐酸和氢氧化钠反应生成碳酸钠和水,碳酸钠溶液和氢氧化钠溶液都是显碱性溶液,都能使酚酞试液变红色,银离子能和氯离子结合生成白色沉淀氯化银,锌能和稀盐酸反应生成氯化锌和氢气.
解答 解:A、混合后溶液的pH值升高了,不能说明盐酸和氢氧化钠发生了反应,这是因为盐酸中加入水时,溶液pH也升高,该选项不能证明二者发生了反应;
B、氢氧化钠溶液显碱性,能使酚酞试液变红色,该选项不能证明二者发生了反应;
C、盐酸能和硝酸银反应生成氯化银沉淀,该选项不能证明二者发生了反应;
D、往反应后溶液中加入金属锌,无任何现象,说明溶液中不含有盐酸,进一步说明盐酸和氢氧化钠发生了反应,该选项能够证明二者确实发生了反应.
故选:D.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
14.常见金属X与硝酸银溶液反应的化学方程式为X+3AgNO3═3Ag+X(NO3)3,有关该反应说法中错误的是( )
| A. | 该反应是置换反应 | B. | 金属活动性X>Ag | ||
| C. | X可能是铁 | D. | X表面有固体覆盖 |
20.正确使用和理解化学用语是重要的学科素养,下列说法正确的是( )
| A. | H2O、H2CO3中均含有氢分子 | |
| B. | H2O和H2O2的组成元素相同,但它们的化学性质不同 | |
| C. | Na+、Mg2+、Al3+原子核内质子数均为10 | |
| D. | 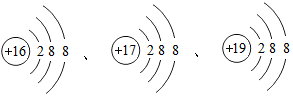 表示的粒子都是阴离子 表示的粒子都是阴离子 |