题目内容
12.如图是元素周期表的一部分: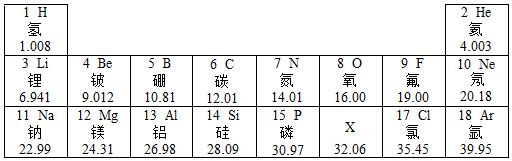
(1)根据周期表规律,表中X是16(填符号)
(2)表中氯元素与一种金属元素组成的化合物共有五种.
(3)元素M的某化合物的化学式为MOH,其相对分子质量为23.941,则M元素的符号是Li.
(4)表中某金属与CuSO4溶液反应后质量增加,请写出可能发生反应的化学方程式(仅写一个)Mg+CuSO4═MgSO4+Cu.
分析 (1)元素周期表中,随原子序数的递增;
(2)根据化合物的形成过程来分析;
(3)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答;
(4)根据金属活动性顺序解答.
解答 解:(1)在元素周期表中,根据同一周期元素原子序数的依次递增的规律,故X介于质子数为15和17之间,为:16;
(2)在化学变化中,金属元素易失去最外层的电子而形成阳离子,可以与氯离子结合成化合物,如氯化锂、氯化铍、氯化钠、氯化镁和氯化铝共五种;故填:五;
(3)元素M的某化合物的化学式为MOH,它的相对分子质量为23.941,则M元素的相对分子质量为:23.941-1-16=6.941,是锂元素,故填:Li;
(4)表中金属镁的活动性大于铜,24份镁参加反应,可以置换出64份铜,反应后质量增加,可能发生反应的化学方程式为::Mg+CuSO4═MgSO4+Cu.
答案:(1)16;(2)五;(3)Li;(4)Mg+CuSO4═MgSO4+Cu.
点评 本题考查学生根据元素周期表中,随原子序数的递增,同一周期元素最外层电子数逐渐增多与质子数与核电荷数的关系进行分析解题的能力.

练习册系列答案
相关题目
13.不同种元素的本质区别是( )
| A. | 质子数不同 | B. | 中子数不同 | ||
| C. | 相对原子质量不同 | D. | 最外层电子数不同 |
3.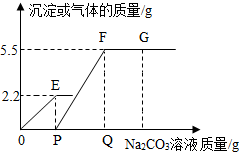 向一定量CaCl2和HCl的混合溶液中,逐渐加入Na2CO3溶液(Na2CO3溶液呈碱性),反应过程中产生气体或沉淀的质量与加入的Na2CO3溶液的质量关系如图,下列说法错误的是( )
向一定量CaCl2和HCl的混合溶液中,逐渐加入Na2CO3溶液(Na2CO3溶液呈碱性),反应过程中产生气体或沉淀的质量与加入的Na2CO3溶液的质量关系如图,下列说法错误的是( )
 向一定量CaCl2和HCl的混合溶液中,逐渐加入Na2CO3溶液(Na2CO3溶液呈碱性),反应过程中产生气体或沉淀的质量与加入的Na2CO3溶液的质量关系如图,下列说法错误的是( )
向一定量CaCl2和HCl的混合溶液中,逐渐加入Na2CO3溶液(Na2CO3溶液呈碱性),反应过程中产生气体或沉淀的质量与加入的Na2CO3溶液的质量关系如图,下列说法错误的是( )| A. | OE有气体生成,生成气体2.2g | |
| B. | PF发生化学反应:Na2CO3+CaCl2═2NaCl+CaCO3↓ | |
| C. | G点溶液的pH=7 | |
| D. | 反应过程有气体和沉淀生成,同样遵循质量守恒定律 |
20.下列化学用语中,既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )
| A. | Ne | B. | H | C. | C60 | D. | 2Fe |
7.下列说法中正确的是( )
| A. | Fe2+、Fe3+都属于铁元素,是同一种离子 | |
| B. | 生石灰和氧化钙都含氧元素和钙元素,是指同一种氧化物 | |
| C. | NO2和N2O4中氮元素的化合价都是+4价,是同一种化合物 | |
| D. | 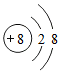 、 、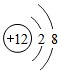 两种粒子的电子排布相同,属于同一种元素 两种粒子的电子排布相同,属于同一种元素 |
17.下列有关燃烧与灭火的说法中错误的是( )
| A. | 用灯帽盖灭酒精灯:隔绝空气 | |
| B. | 森林灭火时,建立隔离带:隔绝可燃物 | |
| C. | 家具起火,用水扑灭:降低温度 | |
| D. | 煤炉生火时,用木柴引燃:提高着火点 |
2.如图所示,主要是依靠空气的浮力而升空的物体是( )
| A. |  同步卫星 同步卫星 | B. |  飞机 飞机 | C. |  风筝 | D. |  氢气球 |
 柑橘是一类美味的水果.如图为某柑橘的部分营养成分
柑橘是一类美味的水果.如图为某柑橘的部分营养成分