题目内容
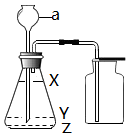
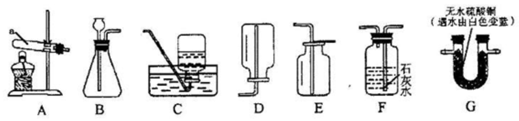
12.以下是实验室制取气体的常用仪器,回答下列问题.
(1)仪器a的名称是锥形瓶;
(2)实验室加热氯酸钾与二氧化锰的混合物制取氧气:
①有关反应的化学方程式为2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;
②组装制取氧气的发生装置,选用的仪器除d、e、g外,还需要选用的一种仪器是f;
(3)若将仪器b、k、l和m组装成收集气体的装置,气体应满足的条件是B.
A.气体密度比空气小 B.气体难(或不易)溶于水 C.气体易溶于水.
分析 (1)熟记仪器的名称;
(2)根据化学反应的原理、化学方程式的写法以及反应物的状态与反应的条件来分析;
(3)根据气体的收集方法决定于气体的密度与水溶性.
解答 解:(1)仪器a是锥形瓶;故填:锥形瓶;
(2)①氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,反应的化学方程式为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑.故答案为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑.
②该反应是固体加热制取氧气,所以选择仪器试管、铁架台、酒精灯、带导管的单孔塞来组装制备装置;故填:f;
(3)仪器b、k、l和m组装成收集气体的装置为排水法,难溶于水或不易溶于水的气体可用排水法收集;故填:B.
点评 本题重点考查了实验室制取氧气的反应方程式、装置、仪器的选取,需要同学们根据所学知识细心考虑;尤其是实验室制取氧气的化学方程式是中考的考查重点.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
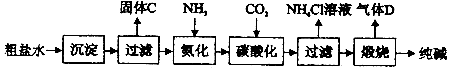
17.我国化学家侯徳榜的“联合制碱法”工艺简洁效率高.其主要反应如下:
①NH3+H2O+CO2═NH4HCO3
②NaCl(饱和)+NH4HCO3═NH4C1+NaHCO3↓
③2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
下列说法正确的是( )
①NH3+H2O+CO2═NH4HCO3
②NaCl(饱和)+NH4HCO3═NH4C1+NaHCO3↓
③2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
下列说法正确的是( )
| A. | ②反应是复分解反应 | |
| B. | ③反应过程中碳元素的化合价发生了改变 | |
| C. | ③反应后的H2O和CO2可以被循环使用 | |
| D. | 反应结束后,只得到一种产物Na2CO3 |
1.下列四位同学分别设计的实验方案,你认为不可行的是( )
| A. | 将pH试纸湿润后,用玻璃棒蘸取食用白醋滴到试纸上,测定其pH | |
| B. | 确定某溶液中是否含有硫酸根离子,可先向该溶液中滴加稀盐酸,若没有任何明显现象,则继续滴加氯化钡溶液,然后观察是否有白色沉淀生成 | |
| C. | 通过灼烧、闻燃烧产生的气味可以鉴别合成纤维与羊毛纤维 | |
| D. | 通过足量灼热的铜网可以除去氮气中混有的少量氧气 |
 化学是一门以实验为基础的学科.
化学是一门以实验为基础的学科.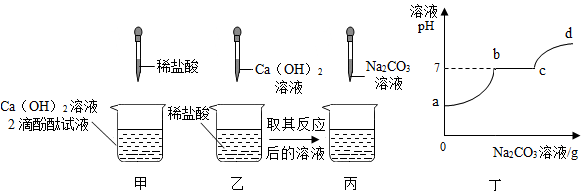
 2016年第17号台风“鲇鱼”给温州市的局部地区带来特大暴雨,导致较严重的内涝灾害,洪灾过后,为防止病菌传染,应对被水淹过的教室等场所进行及时消毒,学校使用过氧乙酸消毒液进行消毒,如图所示是消毒液的标签部分信息,仔细阅读后回答:
2016年第17号台风“鲇鱼”给温州市的局部地区带来特大暴雨,导致较严重的内涝灾害,洪灾过后,为防止病菌传染,应对被水淹过的教室等场所进行及时消毒,学校使用过氧乙酸消毒液进行消毒,如图所示是消毒液的标签部分信息,仔细阅读后回答: