题目内容
16.根据如图所示的实验装置图回答: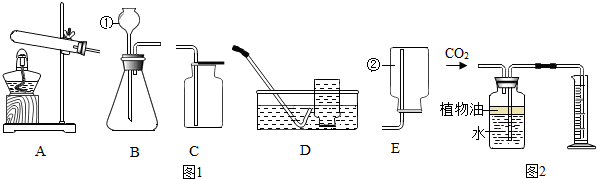
(1)写出编号的仪器名称:①长颈漏斗;②集气瓶;
(2)实验室用高锰酸钾制取氧气时,如果要检验是否有氧气生成,可将带火星的木条接近导管口,如果木条复燃,说明有氧气生成;
(3)实验室常用稀盐酸和石灰石反应制取CO2,该反应的化学方程式为:2HCl+CaCO3═CaCl2+H2O+CO2↑;;制取并收集CO2,应选用的发生装置为B(填序号),收集装置为C(填序号).
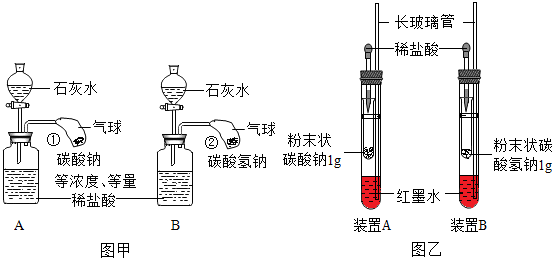
(4)图2所示装置可用来测量生成CO2的体积,其中在水面上放一层植物油的目的是:防止CO2溶解在水中,植物油上方原有的空气对实验结果无(填“有”或“无”)明显影响.
分析 (1)仪器①是长颈漏斗,②是集气瓶;
(2)氧气的特性是使带火星的木条复燃;
(3)制取气体选择发生装置应考虑反应物的状态和反应条件,收集装置应考虑气体的溶水性和密度与空气的大小,实验室常用稀盐酸和石灰石制取二氧化碳,是固体和液体的反应,所以发生装置用B,二氧化碳的密度比空气大,且易溶于水,所以收集装置只能用C;
(4)因为二氧化碳易溶于水,所以水面上放一层植物油的目的是防止二氧化碳溶于水,二氧化碳通入装置内使里面的压强增大,水被压入量筒内,所以里面的气体对实验结果无影响.
解答 解:
(1)①是长颈漏斗;②是集气瓶;
(2)氧气的特性是使带火星的木条复燃,所以答案为:木条复燃;
(3)稀盐酸和石灰石反生成氯化钙、水和二氧化碳,所以方程式为:2HCl+CaCO3═CaCl2+H2O+CO2↑;实验室常用稀盐酸和石灰石制取二氧化碳,是固体和液体的反应,所以发生装置用B,二氧化碳的密度比空气大,且易溶于水,所以收集装置只能用C,故答案为:2HCl+CaCO3═CaCl2+H2O+CO2↑,B,C;
(4)二氧化碳易溶于水,水面上放一层植物油的目的是防止二氧化碳溶于水,二氧化碳通入装置内使里面的压强增大,水被压入量筒内,就可以测出水的体积,即二氧化碳的体积,所以里面的气体对实验结果无影响.
故答案为:防止CO2溶解在水中,无.
答案:
(1))①长颈漏斗;②集气瓶
(2)木条复燃
(3)2HCl+CaCO3═CaCl2+H2O+CO2↑; B C
(4)防止CO2溶解在水中 无
点评 本题考查了氧气和二氧化碳的性质,根据气体的性质选择发生装置,根据反应物的状态和反应条件选择收集装置,以及对两种气体的验满方法等.

练习册系列答案
相关题目
4.下列物质属于纯净物( )
| A. | 液氧 | B. | 新鲜的空气 | C. | 干净的豆浆 | D. | 河水 |
11.对下列现象或做法的解释不正确的是( )
| A. | 洒到地面上的酒会使房间充满酒味,说明分子在不断运动 | |
| B. | 膨化食品变得不再松脆,是因为食品可能吸收了空气中的水分 | |
| C. | 用洗洁精洗去餐具上的油污,是因为洗洁精具有乳化作用 | |
| D. | 消防队员用高压水枪喷水灭火,是因为水能降低可燃物的着火点 |
6.寒假里,小祺的老师布置了一项作业,需要用厨房里的材料完成几个家庭小实验,下面是小祺设计的实验,请问不能成功的是( )
| A. | 用酒精浸泡捣烂的某些植物的花瓣制酸碱指示剂 | |
| B. | 水变油 | |
| C. | 用柠檬酸、果汁、白糖、水、小苏打等制汽水 | |
| D. | 用碎鸡蛋壳和醋精(只要成分是醋酸)制二氧化碳 |