题目内容
13.已知某合金是由四种常见单质组成,通过以下实验和查阅资料已知:①无色气体A能燃烧,产生淡蓝色火焰;
②无色气体F能使澄清石灰水变浑浊.
③该合金不含K、Ca、Na这三种活泼金属;
④几种金属离子的颜色:Fe3+-黄色、Fe2+-浅绿色、Cu2+-蓝色
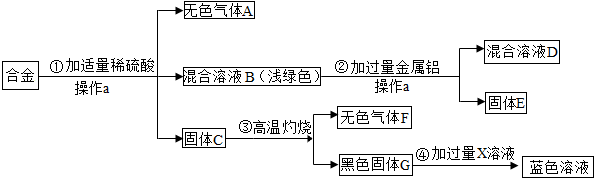
请根据上述实验过程回答以下问题:
(1)合金是由哪几种单质组成:Fe、Cu、C、Mg(均用化学式表示);
写出混合溶液D中一种溶质的名称硫酸镁(硫酸铝).
(2)操作a的名称是过滤,其中需用到的一种玻璃仪器是烧杯(漏斗、玻璃棒).
(3)写出步骤①所涉及的一个化学方程式Fe+H2SO4=FeSO4+H2↑.
(4)步骤④中所加入的X溶液是稀硫酸.步骤④所发生化学反应的基本类型是复分解(选填“化合”、“分解”、“置换”或“复分解”)反应.
分析 根据混合溶液B为浅绿色,可知溶液B中含有亚铁离子,所以合金中有铁,无色气体F能使澄清石灰水变浑浊,所以F是二氧化碳,在空气中充分灼烧会生成二氧化碳,所以合金中有碳,加入稀硫酸得到蓝色溶液,可知黑色固体G是氧化铜,所以合金中有铜,溶液D为混合溶液,可知合金中有比铝化学性质活泼的金属,合金不含K、Ca、Na,且所含金属均在金属活动顺序表中,所以合金中含有的金属就是镁,活泼金属与盐酸反应会生成氢气,所以A是氢气,然后将推出的物质代入转化关系中验证即可.
解答 解:(1)合溶液B为浅绿色,可知溶液B中含有亚铁离子,所以合金中有铁,无色气体F能使澄清石灰水变浑浊,所以F是二氧化碳,在空气中充分灼烧会生成二氧化碳,所以合金中有碳,加入稀硫酸得到蓝色溶液,可知黑色固体G是氧化铜,所以合金中有铜,溶液D为混合溶液,可知合金中有比铝化学性质活泼的金属,合金不含K、Ca、Na,且所含金属均在金属活动顺序表中,所以合金中含有的金属就是镁,活泼金属与盐酸反应会生成氢气,所以A是氢气,经过验证,推导正确,所以合金由Fe、Cu、C、Mg组成,镁会与硫酸反应生成硫酸镁和氢气,铁和稀硫酸反应生成硫酸亚铁和氢气,硫酸是过量的,所以B是硫酸和硫酸亚铁的混合物,铝会与硫酸、硫酸亚铁生成硫酸铝,所以混合溶液中溶质的是:硫酸镁(硫酸铝);
(2)经过操作a得到了溶液B和固体C,所以a是过滤,过滤需要的玻璃仪器有烧杯、漏斗、玻璃棒;
(3)铁和硫酸反应生成硫酸亚铁和氢气,化学方程式为:Fe+H2SO4=FeSO4+H2↑;
(4)黑色固体氧化铜加入x生成了蓝色溶液,故x可以是稀硫酸,稀硫酸与氧化铜的反应是复分解反应;
故答案为:(1)Fe;Cu;C;Mg;硫酸镁;硫酸铝;
(2)过滤;烧杯(漏斗、玻璃棒);
(3)Fe+H2SO4=FeSO4+H2↑;
(4)稀硫酸;复分解.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

| A. | ②④③① | B. | ②③④① | C. | ③②①④ | D. | ③②④① |
 酒精是一种无色、透明、有特殊气味的液体,易挥发,能与水以任意比互溶,常用作酒精灯和内燃机的燃料,是一种绿色能源,当点燃酒精灯时,酒精在灯芯上气化后燃烧生成水和二氧化碳.
酒精是一种无色、透明、有特殊气味的液体,易挥发,能与水以任意比互溶,常用作酒精灯和内燃机的燃料,是一种绿色能源,当点燃酒精灯时,酒精在灯芯上气化后燃烧生成水和二氧化碳.(1)根据以上叙述,可归纳出酒精的物理性质是无色、透明、有特殊气味的液体,易挥发,能与水以任意比互溶;化学性质是能燃烧;酒精的用途是作燃料.
(2)下列仪器不能用酒精灯加热的是C
A.燃烧匙 B.试管 C.量筒 D.蒸发皿
(3)某研究小组在学习氧气的化学性质时发现:铁丝在氧气中燃烧没有火焰,而蜡烛在氧气中燃烧却有明亮的火焰.该小组同学进行了如下探究.
①写出铁丝在氧气中燃烧的符号表达式:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 .
②探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示).由此可知:蜡烛燃烧产生的火焰是由气态(填“固态”或“气态”)物质燃烧形成的.
③探究二:物质燃烧产生火焰的根本原因是什么?
【查阅资料】
| 物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
| 石蜡 | 50∽70 | 300∽550 | 约600 |
| 铁 | 1535 | 2750 | 约1800 |
| 钠 | 97.8 | 883 | 约1400 |
④根据硫在空气或氧气中燃烧的实验事实,请你推测硫沸点<硫燃烧时的温度(填“>”或“<”或“=”)
| A. | 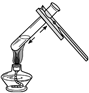 加热液体 | B. | 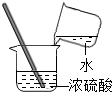 稀释浓硫酸 | C. | 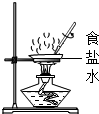 蒸发食盐水 | D. | 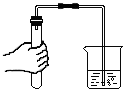 检查装置气密性 |
| A. | 酸性 | B. | 碱性 | C. | 中性 | D. | 无法确定 |
| A. | 摩擦生热 | B. | 二氧化碳的组成元素 | ||
| C. | 水的电解 | D. | 煤的干馏 |
| A. | 铝的元素符号:AL | B. | 2个氢原子:H2 | C. | 钙离子:Ca2+ | D. | 硫酸铁:FeSO4 |