题目内容
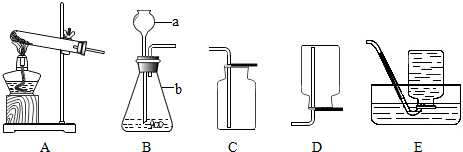
8.下列仪器:①烧杯②量筒③试管④胶头滴管⑤镊子⑥药匙.用序号回答:用来滴加少量液体的是④,取用较大的块状固体药品的是⑤,准确量取 5mL液体的是②④,需要垫加石棉网才能加热的是①.分析 吸取和滴加少量液体的仪器是胶头滴管,取用大块状药品用镊子,量取一定体积的液体用量筒,烧杯不能直接加热,须在下面垫上石棉网.
解答 解:吸取和滴加少量液体的仪器是胶头滴管;
取用较大的块状药品用镊子;
准确量取一定体积的液体用量筒,当接近刻度线时改用胶头滴管进行定容;
可以直接在酒精灯火焰上加热的玻璃仪器是试管,而烧杯在加热时要在底部垫上石棉网,防止给仪器加热不均造成仪器炸裂;
故答案为:④;⑤;②④;①.
点评 本题对常见化学仪器的用途及选取进行了考查,识记性强,难度不大.

练习册系列答案
相关题目
13.下列属于物理变化的是( )
| A. | 切开苹果后,切面不久变黑 | B. | 食物腐败变质 | ||
| C. | 石油通过蒸馏制取汽油 | D. | 铁丝在潮湿的空气中生锈 |
20.分类是学习和研究化学的常用方法,下列物质分类正确的是( )
| A. | 混合物:矿泉水、纯净的空气 | B. | 酸:盐酸、硫酸铜 | ||
| C. | 氧化物:水、氢氧化钠 | D. | 有机物:葡萄糖、二氧化碳 |
17.如图,甲和乙分别是氢气和一氧化碳还原氧化铜的实验,下列有关说法正确的是( )


| A. | 甲实验试管口向下倾斜可防止氢气逸出 | |
| B. | 乙实验只能通过澄清石灰水是否变浑浊判断反应是否发生 | |
| C. | 甲、乙两实验中,都应先通入气体,再使试管、玻璃管均匀受热,以防止发生爆炸 | |
| D. | 甲、乙两实验中,氢气和一氧化碳都将氧化铜变成游离态的铜,都发生了置换反应 |

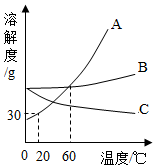 如图为A、B、C三种固体物质的溶解度曲线,回答下列问题:
如图为A、B、C三种固体物质的溶解度曲线,回答下列问题: