题目内容
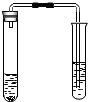
3.某实验小组模拟高炉炼铁的化学反应原理进行实验,其装置如图所示,请回答下列问题.
(1)A处的实验现象是红色固体变成黑色.
(2)B处实验现象是生成白色沉淀.
(3)C处酒精灯的作用是除去尾气中CO(或防止C0使人中毒;防止CO污染空气;将C0转化为没有毒性的C02等合理答案均可).
(4)一种含有铁和氧化铁的混合物与16.8g一氧化碳气体恰好完全反应,其中氧化铁全部被一氧化碳还原,最终所得固体质量为30.4g.则原混合物的质量为40g.
分析 (1)根据一氧化碳还原氧化铁得到铁和二氧化碳的原理分析解答;
(2)二氧化碳能使澄清的石灰水反应;
(3)尾气中含有一氧化碳,必须对尾气进行点燃处理,生成二氧化碳.
(4)根据一氧化碳与氧化铁反应的化学方程式计算出氧化铁的质量,生成铁的质量,然后用最终固体质量减去生成铁的质量就是原固体中铁的质量.
解答 解:(1)在高温条件下,一氧化碳与氧化铁反应生成了了铁和二氧化碳,A处红色的氧化铁还原为黑色的铁,故答案为:红色固体变成黑色;
(2)二氧化碳与氢氧化钙溶液反应生成碳酸钙白色沉淀和水,故填:生成白色沉淀;
(3)一氧化碳有毒,不能直接排放到空气中,因此要在装置图末端的导气管口放一盏燃着的酒精灯将一氧化碳燃烧除去,防止污染空气;故填:除去尾气中CO(或防止C0使人中毒;防止CO污染空气;将C0转化为没有毒性的C02等合理答案均可);
(4)解:设与16.8g一氧化碳气体恰好完全反应需要氧化铁的质量为x,生成铁的质量为y
3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
84 160 112
16.8g x y
$\frac{84}{160}=\frac{16.8g}{x}$
x=32g
$\frac{84}{112}=\frac{16.8g}{y}$
y=22.4g
则原混合物中,铁的质量为:30.4g-22.4g=8g
原混合物的质量为:32g+8g=40g
故填:40.
点评 本题考查了高炉炼铁的原理、实验现象、注意事项以及根据化学方程式的计算,难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
17.2015年娄底市着力打造生态旅游区,下列做法不符合这一主题的是( )
| A. |  爱护花草树木 | B. |  随意排放废水 | C. |  分类回收垃圾 | D. |  绿色低碳出行 |
18.保护空气,使天空更蓝,下列做法不合理的是( )
| A. | 随意大量燃放鞭炮 | B. | 使用绿色公共交通出行 | ||
| C. | 开发和利用各种清洁能源 | D. | 将工业废气处理后再排放 |
8.下列各组物质的溶液,根据它们自身的性质和相互间的反应现象,不用其它试剂就可以加以鉴别的是( )
| A. | FeCl2 NaCl Ba(OH)2 | B. | KCl HCl NaNO3 | ||
| C. | Na2SO4 HCl H2SO4 | D. | CuCl2 NaNO3 K2SO4 |
13.下列属于化学变化的是( )
| A. | 浊液过滤 | B. | 冷却结晶 | C. | 雕石成像 | D. | 铁锅生锈 |
 某化学社团的同学发现,不同物质的变化常伴随着相同的实验现象,但从化学的角度去研究,会发现其有本质的区别.
某化学社团的同学发现,不同物质的变化常伴随着相同的实验现象,但从化学的角度去研究,会发现其有本质的区别.