题目内容
11.实验室常用下列装置来制取氧气: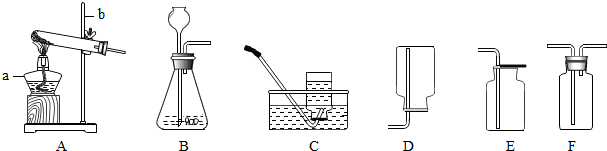
(1)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是B(填序号),其中二氧化锰起催化作用.该反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
(2)用E装置收集氧气的依据是氧气密度比空气大,检验氧气是否集满的方法是将带火星的木条放在集气瓶口,木条复燃,证明集满.
(3)若用加热高锰酸钾的方法制取氧气:若发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是试管口没有放一团棉花;用排水法收集氧气结束时,应先撤导管再熄灭酒精灯;做铁丝在氧气中的燃烧实验时,在集气瓶底部预先留少量水或是铺一层细沙的目的是:防止溅落的熔化物炸裂瓶底
(4)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水,其水溶液呈碱性.
制取氨气反应的方程式:2NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
①制取并收集NH3,应该从如图中选择的发生装置是A,收集装置是D.
②NH3是一种碱性气体,干燥时不能选用下列干燥剂中的B(填序号).
A.固体氢氧化钠 B.浓硫酸 C.生石灰.
分析 (1)根据实验室用过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,二氧化锰是该反应的催化剂,过氧化氢在二氧化锰的催化作用下生成水和氧气进行分析;
(2)根据氧气的密度比空气大,氧气有助燃性进行分析;
(3)根据实验室制取氧气的正确操作进行分析;
(4)根据实验室制取氨气的反应物是固体,反应条件是常温,氨气的密度比空气小易溶于水,氨气是碱性气体,不能用酸性干燥剂进行分析.
解答 解:(1)实验室用过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,所以发生装置选B,二氧化锰是该反应的催化剂,起催化作用,过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)氧气的密度比空气大,所以可以用向上排空气法收集,氧气有助燃性,验满的正确操作是:将带火星的木条放在集气瓶口,木条复燃,证明集满;
(3)用加热高锰酸钾的方法制取氧气:若发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是试管口没有放一团棉花;用排水法收集氧气结束时,应先撤导管再熄灭酒精灯;做铁丝在氧气中的燃烧实验时,在集气瓶底部预先留少量水或是铺一层细沙的目的是:防止溅落的熔化物炸裂瓶底;
(4)实验室制取氨气的反应物是固体,反应条件是常温,氨气的密度比空气小易溶于水,所以选择的发生装置是A,收集装置是D;
氨气是碱性气体,不能用酸性干燥剂,故选:B.
故答案为:(1)B,催化,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)氧气的密度比空气大,将带火星的木条放在集气瓶口,木条复燃,证明集满;
(3)试管口没有放一团棉花;撤导管,熄灭酒精灯;防止溅落的熔化物炸裂瓶底;
(4)A,D;
B.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

| A. | 为人体提供营养物质 | B. | 补充体内盐分 | ||
| C. | 补充体内水分 | D. | 以上三项都是 |
| 反应前物质的质量/g | 充分反应后物质的质量/g | |
| 铁画边角料 | 稀硫酸 | 剩余固体和液体的总质量 |
| 8.5 | 170 | 178.2 |
(2)样品中铁的质量是多少?
(3)样品中金的质量分数是多少?(结果保留一位小数)
| 稀盐酸的用量 | 第一次加入5g | 第二次加入5g | 第三次加入5g | 第四次加人5g |
| 剩余固体的质量 | 3g | 2g | l g | 1g |
(2)4克石灰石中的碳酸钙恰好反应完消耗稀盐酸的质量为15g;.
(3)恰好完全反应后生成二氧化碳多少克?(写出完整解答过程)
| A. |  | B. |  | C. |  | D. | 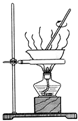 |
| A. | 熔点、沸点 | B. | 颜色、状态 | C. | 可燃性、稳定性 | D. | 密度、硬度 |