题目内容
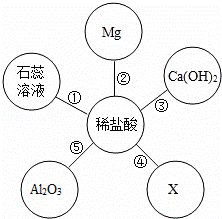
如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同.结合此图回答下列问题:
(1)稀硫酸中阳离子的符号是 ;
(2)反应①中石蕊溶液变为 色;
(3)反应⑤的化学方程式为 ;
(4)图中只生成盐和水的反应有 (填序号);
(5)若X溶液既能跟稀盐酸反应,又能跟Ca(OH)2反应,则X可能是(BaCl2、CuSO4、Na2CO3)中的 .
| 酸的化学性质;书写化学方程式、文字表达式、电离方程式. | |
| 专题: | 常见的酸 酸的通性. |
| 分析: | (1)酸是指在电离时产生的阳离子全部是氢离子的化合物,据此进行分析解答. (2)根据紫色石蕊溶液遇酸溶液变红,遇碱溶液变蓝色,进行分析解答. (3)反应⑤是氧化铝和盐酸反应生成氯化铝和水,写出反应的化学方程式即可. (4)根据各反应的生成物进行分析解答. (5)根据酸、碱的化学性质进行分析解答. |
| 解答: | 解:(1)酸是指在电离时产生的阳离子全部是氢离子的化合物,稀硫酸中阳离子是氢离子,其离子符号为:H+. (2)稀硫酸显酸性,遇石蕊溶液显红色. (3)反应⑤是氧化铝和盐酸反应生成氯化铝和水,反应的化学方程式为:Al2O3+6HCl=2AlCl3+3H2O. (4)③氢氧化钙与稀盐酸反应生成氯化钙和水,⑤氧化铁与稀盐酸反应生成氯化铁和水,生成物均为盐和水,符合题意. (5)BaCl2不能与稀盐酸反应,与Ca(OH)2反应交换成分没有沉淀、气体、水生成,不能发生反应,不符合题意;CuSO4不能与稀盐酸反应,不符合题意;Na2CO3能与稀盐酸反应生成氯化钠、水、二氧化碳,能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,符合题意. 故答案为:(1)H+;(2)红;(3)Al2O3+6HCl=2AlCl3+3H2O;(4)③⑤;(5)Na2CO3. |
| 点评: | 本题难度不是很大,以稀盐酸为例主要考查了酸的化学性质,熟练掌握酸的化学性质是正确解答本题的关键. |

下列各项指定数据前者小于后者的是( )
| 选项 | 数据 | ||
| A | 溶液温度 | 室温下10gNH4NO3溶于100g水中 | 室温下10gNaOH溶于100g水中 |
| B | 物质中氧元素的质量分数 | 甲醛(HCHO) | 葡萄糖(C6H12O6) |
| C | 二氧化碳的溶解度 | 5℃、101KPa下 | 25℃、101KPa下 |
| D | 物质中碳元素的质量分数 | 生铁 | 钢 |
将等质量的CaCO3(块状)和Na2CO3(粉末),分别浸入一定量10%盐酸和10%硫酸溶液中,产生CO2的质量随时间变化曲线如图所示,下列说法正确的是( )

|
| A. | CaCO3一定没有剩余 | B. | 消耗HCl与H2SO4的质量比为73:98 |
|
| C. | 消耗CaCO3与Na2CO3的质量比为1:1 | D. | 反应产生水的质量相等 |
每年6月26日为“国际禁毒日”,下列物质不属于毒品的是( )
|
| A. | 海洛因 | B. | 摇头丸 | C. | 咖啡 | D. | 大麻 |
下列说法中正确的是( )
|
| A. | 水电解生成氢气和氧气,说明水中含有氢分子和氧分子 |
|
| B. | 在水电解的反应中,氢原子和氧原子都没有发生变化 |
|
| C. | 水的蒸发和水的电解都生成气体,它们都是化学变化 |
|
| D. | 物质在变化中所表现出的性质,就是物质的化学性质 |
 (3)人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙
(3)人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙