题目内容
13.某研究小组探究影响过氧化氢分解速率的因素进行了如下实验.记录了各实验的数据如表:实验一
| 实验序号 | 过氧化氢溶液浓度、% | 过氧化氢溶液体积/ml | 温度/C | 二氧化锰的用量/g | 收集氧气的体积/ml | 反应所需的时间/s |
| 1 | 5 | 1 | 20 | 0.1 | 4 | 16.74 |
| 2 | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| 3 | 30 | 5 | 35 | 2 | 49.21 | |
| 4 | 30 | 5 | 55 | 2 | 10.76 |
(2)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总质量不变(选填“减小”或“不变”或“增大”).
资料信息:聪敏同学在网上查阅资料得知:Cu2+、Fe3+对H2O2分解也具有催化作用.
实验二
为比较Fe3+和Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验.回答相关问题:
(3)定性分析:如图甲可通过观察反应产生气泡的快慢,定性比较得出结论.
有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是控制阴离子相同,排除阴离子的干扰.
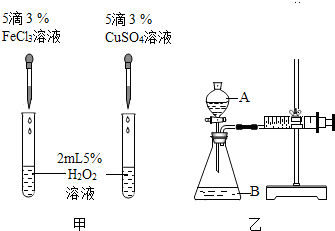
(4)定量分析:如图乙所示进行实验,在装药品前应该检查装置的气密性,具体做法是:将注射器活塞向外拉出一段,松开手一会儿后,若活塞又回到原位,证明装置气密性良好,若实验时均以生成30mL气体为准,其他可能影响实验的因素均已忽略,实验中需要测量的数据是收集30mL气体所需要的时间.
(5)写出图甲任一反应的化学方程式:2H2O2$\frac{\underline{\;FeCl_{3}\;}}{\;}$2H2O+O2↑.
分析 ①②是过氧化氢浓度不同而其他条件相同,这种设计是验证反应物浓度对反应速度的影响;③④则是温度不同其他条件相同,是对温度影响化学反应速度的探究.加水稀释不会改变生成氧气的质量;根据对照实验变量的唯一性分析;根据检查装置气密性的方法进行分析解答;根据化学方程式的书写方法解答.
解答 解:(1)从表中分析可知:①②是过氧化氢浓度不同而其他的反应时各种量均相同,可知这一过程是考查反应物的浓度与反应速度的关系;③④则是温度不同其他条件相同,明显是对温度影响化学反应速度的探究.故填:过氧化氢浓度越大;当反应温度越高时,过氧化氢分解速率越大;
(2)加水稀释不会改变生成氧气的质量,故填:不变;
(3)要比较催化效果,可以通过观察产生气泡的快慢进行,故填:反应产生气泡的快慢;
(4)要检查装置的气密性,可以将注射器活塞向外拉出一段,松开手一会儿后,若活塞又回到原位,证明装置气密性良好;实验时均以生成30mL气体为准,实验中需要测量收集30 mL气体所需要的时间,故填:将注射器活塞向外拉出一段,松开手一会儿后,若活塞又回到原位,证明装置气密性良好;收集30 mL气体所需要的时间;
(5)过氧化氢在氯化铁的催化作用下能分解生成水和氧气,故填:2H2O2$\frac{\underline{\;FeCl_{3}\;}}{\;}$2H2O+O2↑.
点评 本题主要考查了能够影响化学反应的因素,解答这类题时要注意尽可能的把题中的能够影响化学反应的因素找出,然后再利用控制变量法来进行判断,最后得出答案.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
8.下列物质间的转化,在一定条件下均能一步实现的是( )
①C→CO→CO2
②H2O2→H2O→O2
③Na2CO3→NaCl→NaNO3
④CaCO3→CaO→Ca(OH)2.
①C→CO→CO2
②H2O2→H2O→O2
③Na2CO3→NaCl→NaNO3
④CaCO3→CaO→Ca(OH)2.
| A. | ①②③ | B. | ①③④ | C. | ①②④ | D. | ①②③④ |
2.归纳与比较是化学学习的主要方法,有关CO、CO2的不同点比较错误的是( )
| A. | 构成:一个二氧化碳分子比一个一氧化碳分子多一个氧原子 | |
| B. | 性质:CO2能溶于水,但和水不发生化学反应;CO难溶于水,但能燃烧 | |
| C. | 用途:CO2可用于光合作用、灭火;CO可作气体燃料,还可用于冶炼金属 | |
| D. | 危害:CO2会造成温室效应,CO易与血液中的血红蛋白结合引起中毒 |
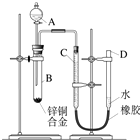 某学习小组用如右图所示装置测定锌铜合金中锌、铜的质量分数.
某学习小组用如右图所示装置测定锌铜合金中锌、铜的质量分数. 小明用六块A~F分别对应铁、二氧化碳、硫酸、氢氧化钙、碳酸钠、氯化钡的积木,按照物质能反应积木就叠放在一起,不反应积木间就不接触的原则,搭成如图所示形状.已知E的物质类别与其他5种不同,B与C反应可以生成F,请完成下列问题:
小明用六块A~F分别对应铁、二氧化碳、硫酸、氢氧化钙、碳酸钠、氯化钡的积木,按照物质能反应积木就叠放在一起,不反应积木间就不接触的原则,搭成如图所示形状.已知E的物质类别与其他5种不同,B与C反应可以生成F,请完成下列问题: 如图为元素周期表中钚元素的相关信息,下列关于钚的说法正确的是B.
如图为元素周期表中钚元素的相关信息,下列关于钚的说法正确的是B.