题目内容
11.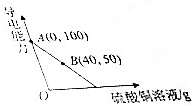 已知向100g氢氧化钡溶液中滴加溶质质量分数为10%的硫酸铜溶液,溶液的导电能力随着硫酸铜溶液的加入发生如图的变化关系.
已知向100g氢氧化钡溶液中滴加溶质质量分数为10%的硫酸铜溶液,溶液的导电能力随着硫酸铜溶液的加入发生如图的变化关系.(1)溶液处于B点时,其中含有的是Ba2+、OH-、H2O(填微粒符号),此时若向溶液中滴加酚酞试液呈红色.
(2)计算氢氧化钡溶液的溶质质量分数.
分析 氢氧化钡溶液与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钡沉淀,至恰好完全反应,溶液的导电性为0;由图示可知,溶液处于B点时,导电能力由100变为50,说明参加反应的氢氧化钡溶液为原溶液的一半,此时消耗的硫酸铜溶液的质量为40g,则恰好完全反应时,消耗的硫酸铜溶液的质量应为80g,由硫酸铜溶液溶质质量分数为10%,根据反应的化学方程式列式计算出参加反应的氢氧化钡的质量,进而计算出氢氧化钡溶液的溶质质量分数.
解答 解:(1)氢氧化钡溶液与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钡沉淀,溶液处于B点时,导电能力由100变为50,说明参加反应的氢氧化钡溶液为原溶液的一半,此时溶液中的溶质为氢氧化钡,氢氧化钡是由钡离子和氢氧根离子构成的,水是由水分子构成的,其符号分别是Ba2+、OH-、H2O;此时溶液显碱性,若向溶液中滴加酚酞试液呈红色.
(2)溶液处于B点时,导电能力由100变为50,此时消耗的硫酸铜溶液的质量为40g,则恰好完全反应时,消耗的硫酸铜溶液的质量应为80g.
设参加反应的氢氧化钡的质量为x
Ba(OH)2+CuSO4=Cu(OH)2↓+BaSO4↓
171 160
x 80g×10%
$\frac{171}{160}=\frac{x}{80g×10%}$ x=8.55g
氢氧化钡溶液的溶质质量分数为$\frac{8.55g}{100g}$×100%=8.55%.
答:(1)Ba2+;OH-;H2O;红;(2)氢氧化钡溶液的溶质质量分数为8.55%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.下列选项中物质的名称,俗名,化学式不一致的是( )
| A. | 氧化钙 生石灰CaO | B. | 碳酸钠 纯碱 Na2CO3 | ||
| C. | 银 水银 Ag | D. | 氢氧化钠 苛性钠NaOH |
19.下列图示的实验操作,正确的是( )
| A. | 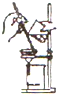 过滤 | B. | 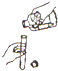 倾倒液体 | C. | 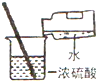 稀释浓硫酸 | D. | 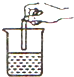 测定溶液的pH |
3.下列物质的性质中,属于物理性质的是( )
| A. | 鉴别真假黄金可用灼烧法 | B. | 物质挥发性 | ||
| C. | 物质可燃性 | D. | 物质氧化性 |
10.向CuO和铁粉的混合物中加入一定量的稀硫酸,微热,充分反应后冷却,过滤,在滤液中放入一枚洁净的铁钉,发现铁钉表面无任何变化,据此判断下列结论正确的是( )
| A. | 滤液中一定含有FeSO4 可能含有H2SO4 | |
| B. | 滤液中可能含有CuSO4 | |
| C. | 滤渣里一定有Fe 和Cu | |
| D. | 滤渣里一定有 Cu 可能有 Fe和CuO |
8.下列离子能在水溶液中大量共存的一项是( )
| A. | Fe3+、K+、NO3-、OH- | B. | H+、Na+、HCO3-、Cl- | ||
| C. | Ag+、NH4+、Cl-、SO42- | D. | Na+、K+、NO3-、CO32- |