题目内容
5.鉴别如表物质的方法不正确的是( )| 选项 | 鉴别的物质 | 鉴别的方法 |
| A | 冰和干冰 | 室温(20℃)放置一会,观察是否有痕渍 |
| B | 水和双氧水 | 加二氧化锰,观察是否有气泡 |
| C | 硬水和软水 | 加入肥皂水,观察产生泡沫的多少 |
| D | 二氧化锰和四氧化三铁 | 观察颜色 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据干冰是固态二氧化碳,冰是固态的水进行分析;
B、根据二氧化锰能催化过氧化氢分解生成氧气进行分析;
C、根据硬水和软水的鉴别进行分析;
D、根据物质的颜色进行分析.
解答 解:A、取样品,室温放置,过一段时间观察有液体残留的是冰,没有残留的是干冰,现象不同,可以鉴别,故A正确;
B、取样品,加入二氧化锰,有气泡产生的是过氧化氢溶液,没有明显现象的是水,现象不同,可以鉴别,故B正确;
C、硬水与肥皂水混合产生浮渣,软水与肥皂水混合产生泡沫,故C正确;
D、二氧化锰和四氧化三铁都是黑色的固体,观察颜色无法鉴别,故D错误.
故选:D.
点评 在解此类题时,首先分析被鉴别物质的性质,然后选择适当的试剂和方法,出现不同的现象即可鉴别.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.溶液与人类生活息息相关,溶液的配制是日常生活和化学实验中常见的操作,表是硫酸溶液和氨水的密度与其溶质质量分数对照表(20℃)
(1)氨水的密度与溶液中溶质质量分数的关系是氨水的密度随着溶液中溶质的质量分数的增大而减小;
(2)向10g28%的硫酸溶液中加水60g,摇匀,所得溶液的体积约是68.6mL(保留一位小数)
| 溶液中溶质的质量分数/% | 4 | 12 | 16 | 24 | 28 |
| 硫酸溶液的密度/g/cm3 | 1.02 | 1.08 | 1.11 | 1.17 | 1.20 |
| 氨水的密度/g/cm3 | 0.98 | 0.95 | 0.94 | 0.91 | 0.90 |
(2)向10g28%的硫酸溶液中加水60g,摇匀,所得溶液的体积约是68.6mL(保留一位小数)
16.人们在如图所示的活动或操作过程中,发生化学变化的是( )
| A. | 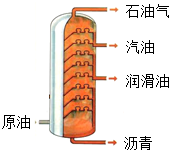 石油分馏 | B. | 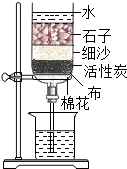 净化水 | ||
| C. | 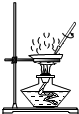 蒸发食盐水 | D. | 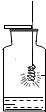 铁丝在氧气中燃烧 |
20.将下列固体加入稀硫酸中,溶液的酸性不会明显减弱的是( )
| A. | Zn | B. | BaCl2 | C. | NaOH | D. | CaO |
14.我国历史上爆发了有名的“鸦片战争”,鸦片屡禁不止,是由于易于吸食上瘾,其可能原因是( )
| A. | 鸦片味道好,是著名的美味剂 | |
| B. | 人由于心理失去平衡,追求某种特殊剌激 | |
| C. | 鸦片中存在的吗啡的分子结构与人脑中的分泌物脑肽的分子结构相近 | |
| D. | 生成鸦片的花罂粟很美 |
9.NaOH溶液可使无色酚酞变红.我们知道NaOH溶液中含有Na+离子、OH-离子、H2O分子,如要探究是哪种微粒使酚酞变红,请填写如表内容:
| 实验步骤 | 现象 | 分析推理过程 | 结论 |
| (1)向盛有氯化钠溶液的试管中滴加几滴酚酞试液; (2)向盛有氢氧化钠溶液的试管中滴加几滴酚酞试液 | (1)酚酞试液不变色; (2)酚酞试液变红色; | 氯化钠溶液中含有钠离子、氯离子和水分子,由实验现象可知,钠离子和水分子不能使酚酞试液变色; 氢氧化钠溶液中含有氢氧根离子,钠离子和水分子,由实验现象可知,氢氧根离子能使酚酞试液变色. | 氢氧化钠溶液中能使酚酞试液变色的是氢氧根离子. |
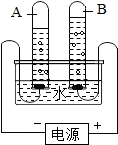 电解水的实验,如图装置,会带下列问题:
电解水的实验,如图装置,会带下列问题: