题目内容
老师请化学兴趣小组的同学帮助他将失去标签的碳酸钠、稀盐酸、氯化钠、氢氧化钠和氯化钙溶液鉴别出来.重新贴好标签.为了区分这五种溶液,将试剂瓶编号为A,B,C,D,E,该小组同学进行了如下探究:
实验步骤 实验现象 实验结论
步骤一 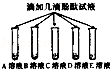 B,C溶液呈现红色
B,C溶液呈现红色
A,D,E溶液颜色无明显变化 B,C溶液显 性
步骤二 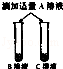 B,C溶液红色均消失,
B,C溶液红色均消失,
且C溶液中产生大量气泡 可确定B为
溶液;A与C的反应通常
不用作实验室制取气体的
原因是
步骤三 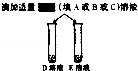
E中无明显现象,
D中的现象为
确定E为氯化钠溶液,
则D溶液与所加试剂发生反应的化学方程式为
实验步骤 实验现象 实验结论
步骤一 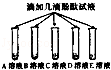 B,C溶液呈现红色
B,C溶液呈现红色
A,D,E溶液颜色无明显变化 B,C溶液显 碱 性
步骤二  B,C溶液红色均消失,
B,C溶液红色均消失,
且C溶液中产生大量气泡 可确定B为
氢氧化钠 溶液;A与C的反应通常
不用作实验室制取气体的
原因是
反应速率太快
步骤三  C
E中无明显现象,
C
E中无明显现象,
D中的现象为
产生白色沉淀 确定E为氯化钠溶液,
则D溶液与所加试剂发生反应的化学方程式为
CaCl2+Na2CO3═CaCO3↓+2NaCl
【解析】
试题分析:步骤一:向溶液中滴加酚酞,B,C溶液呈现红色,说明BC溶液呈碱性,是氢氧化钠和碳酸钠溶液;步骤二:向氢氧化钠和碳酸钠溶液中滴加A,B,C溶液红色均消失,且C溶液中产生大量气体,说明滴加的A溶液与BC能反应,据碳酸盐遇酸生气的特点,可知A是稀盐酸,B是氢氧化钠溶液,碳酸钠和稀盐酸反应速率太快,不利于收集,故不能用来收集二氧化碳;步骤三:DE分别是氯化钠、氯化钙,氯化钠与ABC均不发生反应,氯化钙能与碳酸钠反应生成碳酸钙沉淀,反应方程式是:CaCl2+Na2CO3═CaCO3↓+2NaCl;故滴加碳酸钠可将二者区分开;
考点:酸、碱、盐的鉴别



