题目内容
15.浓硫酸有较强的腐蚀性,在稀释和使用时要特别小心.以下是稀释浓硫酸的操作,规范的是( )| A. | 稀释浓硫酸时,把水慢慢倒入盛有浓硫酸的烧杯中 | |
| B. | 为了防止手沾到硫酸,稀释时不要搅拌 | |
| C. | 将浓硫酸沿着烧杯内壁慢慢注入水中,并不断搅拌 | |
| D. | 不慎把浓硫酸洒在皮肤上,用氢氧化钠溶液中和 |
分析 根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)、浓硫酸不慎沾到皮肤上的处理方法,进行分析判断.
解答 解:A、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中,故选项说法错误.
B、为使热量及时地扩散,稀释时要用玻璃棒不断搅拌,故选项说法错误.
C、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中,故选项说法正确.
D、浓硫酸具有较强的腐蚀性,不慎沾到皮肤上,应立即用大量清水冲洗,后涂上3%~5%的碳酸氢钠溶液,不能用氢氧化钠溶液中和,因为氢氧化钠具有强烈的腐蚀性,故选项说法错误.
故选:C.
点评 本题难度不大,掌握浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)、浓硫酸不慎沾到皮肤上的处理方法是正确解答本题的关键.

练习册系列答案
相关题目
6.物质分类的方法很多,有同学将CO2、CO、SO2归为一类,将CaO、Fe2O3、CuO归为另一类.他进行这样的分类不可能是依据( )
| A. | 颜色 | B. | 溶解性 | C. | 元素组成 | D. | 状态 |
3. 等质量的两种常见金属A和B,分别与足量的稀硫酸反应,生成正二价的 金属硫酸盐和氢气.生成氢气的质量与时间关系如图,请结合所学知识回答:
等质量的两种常见金属A和B,分别与足量的稀硫酸反应,生成正二价的 金属硫酸盐和氢气.生成氢气的质量与时间关系如图,请结合所学知识回答:
(1)最终反应结束后,生成氢气的质量A比B多,这又说明A的相对原子质量比B的相对原子质量小.(填“大”或“小”)
(2)根据曲线可以看出:金属A的活动性比金属B的活动性弱(填“强”或“弱”)
(3)某同学进行了多次金属与足量酸反应的实验,记录了如下一组数据:
根据上表信息,你能得出当金属与足量的酸反应时,生成1克氢气需要金属的质量规律为$\frac{金属的质量(数值上等于相对原子量)}{价数}$.
 等质量的两种常见金属A和B,分别与足量的稀硫酸反应,生成正二价的 金属硫酸盐和氢气.生成氢气的质量与时间关系如图,请结合所学知识回答:
等质量的两种常见金属A和B,分别与足量的稀硫酸反应,生成正二价的 金属硫酸盐和氢气.生成氢气的质量与时间关系如图,请结合所学知识回答:(1)最终反应结束后,生成氢气的质量A比B多,这又说明A的相对原子质量比B的相对原子质量小.(填“大”或“小”)
(2)根据曲线可以看出:金属A的活动性比金属B的活动性弱(填“强”或“弱”)
(3)某同学进行了多次金属与足量酸反应的实验,记录了如下一组数据:
| 实验情况/金属质量 | 27克铝 | 24克镁 | 56克铁 | 65克锌 |
| 相对原子质量 | 27 | 24 | 56 | 65 |
| 金属化合价 | +3 | +2 | +2 | +2 |
| 产生氢气质量/克 | 3 | 2 | 2 | 2 |
10.下列物质中,不属于碱的是( )
| A. | 纯碱 | B. | 氢氧化镁 | C. | 熟石灰 | D. | 烧碱 |
20.关于电解水的实验,下列说法中正确的是( )
| A. | 水分解成氢气和氧气的过程是物理变化 | |
| B. | 和负极相通的玻璃管内生成的气体是氧气 | |
| C. | 和正极相通的玻璃管内生成的气体是氢气 | |
| D. | 这个实验说明了水是由氢元素和氧元素组成的 |
7.目前从海水中提取食盐的方法主要是利用海水晒盐,它所利用的物质分离方法是( )
| A. | 过滤法 | B. | 蒸发溶剂结晶法 | C. | 降温结晶法 | D. | 蒸馏法 |
4.滴有酚酞试液的氢氧化钙溶液与下列物质恰好完全反应后,溶液仍能显红色的是( )
| A. | 盐酸 | B. | 硫酸 | C. | 二氧化碳 | D. | 碳酸钾 |
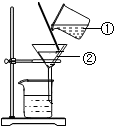 如图为精制粗盐时过滤装置的示意图,请回答:
如图为精制粗盐时过滤装置的示意图,请回答: