题目内容
6.曲酸(C6H6O4)是一种新型添加剂,它具有广泛的抗菌作用,作为防腐剂添加于食品中,具有非常好的效果.试计算:(1)曲酸中C、H、O的质量比36:3:32
(2)14.2克曲酸中碳元素的质量是7.2 克..
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)曲酸中C、H、O的质量比是(12×6):(1×6):(16×4)=36:3:32.
(2)14.2克曲酸中碳元素的质量是14.2g×$\frac{12×6}{12×6+1×6+16×4}$×100%=7.2g.
故答案为:(1)36:3:32;(2)7.2g;
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
14.下列有关量的变化图象与其对应叙述相符的是( )
| A. | 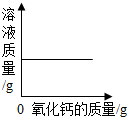 常温下,向一定量的饱和石灰水中加入氧化钙 常温下,向一定量的饱和石灰水中加入氧化钙 | |
| B. | 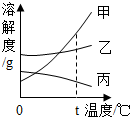 t℃时,向等质量的甲、乙、丙三种物质中分别加水配成饱和溶液,所得溶液质量最小的是丙 t℃时,向等质量的甲、乙、丙三种物质中分别加水配成饱和溶液,所得溶液质量最小的是丙 | |
| C. | 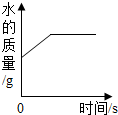 向一定质量的过氧化氢的水溶液中加入二氧化锰 向一定质量的过氧化氢的水溶液中加入二氧化锰 | |
| D. | 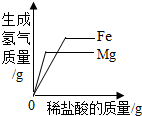 向等质量的铁和镁中分别加入足量的稀盐酸 向等质量的铁和镁中分别加入足量的稀盐酸 |
17.“黄金有价,玉无价”,某玉石的主要成分为NaAlSi2O6,关于NaAlSi2O6的说法正确的是( )
| A. | 该物质含3种金属元素 | B. | 其中硅元素的化合价为+4价 | ||
| C. | 该物质由10个原子构成 | D. | 其相对分子质量为202克 |
14.下列有关物质组成的说法正确的是( )
| A. | 葡萄糖是一种无机物 | |
| B. | 天然气、氢气都属于含碳燃料 | |
| C. | 造成酸雨的主要物质是二氧化碳和二氧化硫 | |
| D. | 煤气是由一氧化碳、甲烷、氢气组成的混合物 |
1.下列原子中的粒子,带负电荷的是( )
| A. | 原子核 | B. | 电子 | C. | 质子 | D. | 中子 |
11.下列是同学测定的某实验滤液中大量存在的成分,其中合理的是( )
| A. | Na+,Ba2+,SO42- | B. | H+,Cu2+,OH- | C. | K+,OH-,Cl- | D. | H+,CO32-,Cl- |
18.下列物质中属于纯净物的是( )
| A. | 碘酒 | B. | 黄铜 | C. | 氧气 | D. | 石油 |
15.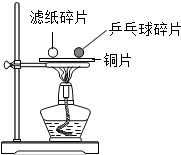 如图所示,把同样大小的滤纸碎片和乒乓球碎片分开放在一块薄铜片的两侧,加热铜片的中部,下列实验现象或结论错误的是( )
如图所示,把同样大小的滤纸碎片和乒乓球碎片分开放在一块薄铜片的两侧,加热铜片的中部,下列实验现象或结论错误的是( )
 如图所示,把同样大小的滤纸碎片和乒乓球碎片分开放在一块薄铜片的两侧,加热铜片的中部,下列实验现象或结论错误的是( )
如图所示,把同样大小的滤纸碎片和乒乓球碎片分开放在一块薄铜片的两侧,加热铜片的中部,下列实验现象或结论错误的是( )| A. | 实验中使用铜片,是利用了铜的导热性 | |
| B. | 铜片受热的一面变黑,是因为产生了CuO | |
| C. | 实验过程中滤纸碎片先燃烧,乒乓球碎片后燃烧 | |
| D. | 实验说明燃烧的条件之一是温度达到可燃物的着火点 |
3.甲和乙在一定条件下恰好完全反应生成丙和丁.结合微观示意图分析,下列结论正确的是( )


| A. | 甲的化学式为H2O | |
| B. | 反应中甲、乙、丁的分子个数比为1:2:1 | |
| C. | 若32g乙参加反应,则生成18g丁 | |
| D. | 丁中氧元素的质量一定等于参加反应的乙的质量 |