题目内容
17.实验室用碳酸钙与稀盐酸反应制8.8克CO2需CaCO3多少克?分析 根据制取二氧化碳的质量,根据碳酸钙与稀盐酸反应的化学方程式可以列式计算即可.
解答 解:设需碳酸钙质量为x.
2HCl+CaCO3=CaCl2+H2O+CO2↑
100 44
x 8.8g
$\frac{100}{x}=\frac{44}{8.8g}$
x=20g
答案:需碳酸钙质量为20g.
点评 本题难度不大,考查物质的化学方程式的计算,根据计算格式解答此类题即可.

练习册系列答案
相关题目
8.下列关于催化剂的说法错误的是( )
| A. | 催化剂在反应前后的质量保持不变 | |
| B. | MnO2可作H2O2分解制O2过程的催化剂 | |
| C. | 催化剂都加快反应速率 | |
| D. | 催化剂实际上也参加到反应过程之中 |
5.下列各种盐能够溶解在水中的是( )
| A. | 食盐 | B. | 碳酸钙 | C. | 碳酸钡 | D. | 硫酸钡 |
2.已知碳有如下反应:H2O+C$\frac{\underline{\;高温\;}}{\;}$CO+H2,据此推测湿煤燃烧产生的火焰与干煤燃烧的火焰比较,现象是( )
| A. | 更旺 | B. | 更弱 | C. | 熄灭 | D. | 无变化 |
7.下列分离混合物的方法中,所依据的原理错误的是( )
| A. | 分离制氧气后剩余固体中的二氧化锰和锰酸钾--利用二氧化锰和锰酸钾的溶解性不同 | |
| B. | 将石油加热炼制,可得到汽油、煤油、柴油等产品--利用石油中各成分的沸点不同 | |
| C. | 分离硝酸钾和氯化钠组成的混合物--利用两者溶解度受温度影响不同 | |
| D. | 分离液态空气制取氧气--利用氮气和氧气的密度不同 |
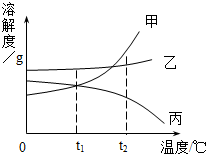 如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在),请根据如图回答:
如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在),请根据如图回答: 如图是厨房的一角.请根据图中所标物品名称回答下列问题:
如图是厨房的一角.请根据图中所标物品名称回答下列问题: