��Ŀ����
������ˮ�Ǿ����ճ��������ų��ķ�ˮ����Ҫ��Դ��סլ�����ء�ѧУ��ҽԺ�̵ꡢ������������ҵ��ҵ������ȡ�������ˮ�жຬ�����ס����Ԫ�غ��²�ϸ���������������ˮ�����Ҫ��ȾԴ֮һ����ˣ�������ˮ�ŷ�ǰ������д�����
�ִ���ˮ�����������������̶Ȼ��֣��ɷ�Ϊһ���������������������ա���ˮһ������Ӧ��������������ɸ�ˡ�������ȥ����ˮ�в��ܽ���������ݺ��ม���ʡ���ˮ����������Ҫ��Ӧ�����ﴦ����������ͨ������Ĵ�л���ý�������ת���Ĺ��̣�����ˮ�еĸ��ָ��ӵ��л�����������Ϊ�����ʡ���ˮ������������һ�����������Ļ����ϣ�Ӧ�û��������ˡ����ӽ�������������������ѧ����ȥ����ˮ�����ܽ���л���ס�����Ӫ�������ʡ���ˮ�е���Ⱦ����ɷdz����ӳ�����Ҫ���ϼ��ַ�����ϣ����ܴﵽ����Ҫ��
��ˮ�����豸�������ˮ��Ҳ������ˮ������ˮ�ʽ�����ˮ������ˮ֮�䣬����һ����Χ��ʹ�õķ�����ˮ��
��1��д��������ˮ������Ԫ�ص�Ԫ�ط���_____������д���֣�
��2��д������ˮ���������У�Ӧ���˵���������_____����д��һ�֣�
��3������ˮ����_____��������������
��4������Ϊ����ˮ�ڹ�ũҵ����������������Щ��;_____��
ij��ѧ�С�����ѧϰ�������ƺ��������Ƶ����֪ʶ�������Ca��OH��2��NaOH���ܽ�����ݡ���ش��������⣺
�¶�/�� | 0 | 20 | 40 | 60 | 80 | 100 | |
�ܽ��/g | Ca��OH��2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 |

��1�������ϱ����ݣ�������Ca��OH��2��NaOH���ܽ�����ߣ�ͼ���ܱ�ʾNaOH�ܽ�����ߵ���_____���A����B������
��2����һƿ�ӽ����͵�Ca��OH��2��Һ��ɱ�����Һ�������ʩ�У�
�ټ��������������Ƣ������¶Ȣ۽����¶Ȣܼ���ˮ������ˮ���ٻָ���ԭ�¶Ȣ���������ʯ�ҡ�
���д�ʩ��ԭ������ȷ����_____������ĸ��
A �ڢܢ� B �ۢ� C �٢ڢݢ� D �٢ڢ�
��3��20��ʱ��191g����NaOH��Һ������10gˮ���ٻָ���20�棬������NaOH���塣��ʱ��Һ����������Ϊ_____
��4��20��ʱ�����ⶨNaOH��Һ��pH�����Ƚ�pH��ֽ������ˮ��ʪ���ٽ��вⶨ����������Һ��pH_____���ƫ��ƫС��������Ӱ�족����
��5���ɼ�������������Һ�ͳ���ʯ��ˮ��һ����ѧ��Ӧ����ʽΪ_____��
��ѧ���ϣ�ͬѧ�ǶԷ��ӵ�����չ������̽����
���龰���裩
�龰1����ʦ������������һЩ��ˮ������һ�����ͬѧ�Ƕ��ŵ�����ζ��
�龰2�����Ͻ��ܣ�������ˮ�ݲ裬3��4���Ӻ������Ϳڸ���ѡ����俪ˮ�ݲ裬Լ8��10Сʱ��ζ�ʴ��ɿڡ�
��������⣩�����龰˵�����Ӿ���ʲô�����أ�
���������룩����һ������֮���м����
������������ڲ�ͣ���˶������¶�Խ�ߣ������˶�Խ�졣
������ʵ�飩
ʵ�鲽�� | ʵ������ | ʵ����� |
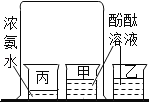
����һ�� �����ͼ��ʾ��ʵ�飬����һ��ʱ���۲졣 ��ʾ����1������ˮ�ǰ�������ˮ�γɵġ� ��2������̪��Һ����ˮ�� ��3������ˮ��ʹ��̪��Һ��졣 | ʵ������______ | �������ȷ |
���������������������Ʒ��ͬʱ����ֱ� ʢ��_____��A��B���ձ��У�����һ��ʱ���۲졣��ͼ��ʾ�� ��ʾ��Ʒ��������ˮ���γɺ�ɫ��Һ | ʵ������ ______ |
��ʵ�鷴˼�������л��������������¶�Ӱ������˶����ʵ����������һ����_____��