题目内容
5.硅是信息技术的关键材料,高温下氢气与四氯化硅(SiCl4)反应可制得高纯度的硅,反应的化学反应方程式为:2H2+SiCl4$\frac{\underline{\;高温\;}}{\;}$Si+4X,下列说法不正确的是( )| A. | X的化学式为HCl | |
| B. | 该反应是置换反应 | |
| C. | 四氯化硅是由一个硅原子和四个氯原子构成 | |
| D. | 四氯化硅中硅元素和氯元素的质量比为14:71 |
分析 A、根据质量守恒定律的元素守恒、原子种类和个数不变,结合反应的化学方程式为:2H2+SiCl4$\frac{\underline{\;高温\;}}{\;}$Si+4X,推测物质X的有关信息.
B、考虑置换反应的特点进行分析;
C、考虑分子的构成;
D、根据硅元素和氯元素的相对原子质量结合四氯化硅的化学式求算出硅元素和氯元素的质量比.
解答 解:
A、根据质量守恒定律的元素守恒、原子种类和个数不变,结合反应的化学方程式为:2H2+SiCl4$\frac{\underline{\;高温\;}}{\;}$Si+4X,反应前H原子个数为4个,Si原子个数为1个,Cl原子个数为4个;反应后Si原子个数为1个,故推测X中有1个H原子和1个Cl原子,为HCl.故正确;
B、反应物和生成物都是一种单质和一种化合物,属于置换反应.故正确;
C、一个四氯化硅分子是由一个硅原子和四个氯原子构成,故原说法错误;
D、四氯化硅中硅元素和氯元素的质量比为=28:(35.5×4)=14:71,故正确.
故选:C.
点评 解答本题关键是要知道置换反应的特点和发生反应需要满足的条件、利用化学式的特点进行处理.

练习册系列答案
相关题目
15.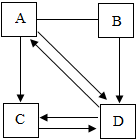 化学兴趣小组的同学在老师的指导下,开展如下探究活动.
化学兴趣小组的同学在老师的指导下,开展如下探究活动.
探究:A、B、C、D分别是碳酸钠、氢氧化钠、氢氧化钙、硫酸钠中的一种,它们之间的转化关系如图所示.(“→”表示物质之间的转化关系,“-”表示物质之间可以发生化学反应)
(1)四种物质中,属于盐类的物质是Na2SO4、Na2CO3(填化学式,下同)
(2)物质D是NaOH.
 化学兴趣小组的同学在老师的指导下,开展如下探究活动.
化学兴趣小组的同学在老师的指导下,开展如下探究活动.探究:A、B、C、D分别是碳酸钠、氢氧化钠、氢氧化钙、硫酸钠中的一种,它们之间的转化关系如图所示.(“→”表示物质之间的转化关系,“-”表示物质之间可以发生化学反应)
| OH- | NO3- | Cl- | SO42- | CO32- | |
| H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 溶 | 微 | 溶 |
| Ba2+ | 溶 | 溶 | 溶 | 不 | 不 |
| Mg2+ | 不 | 溶 | 溶 | 溶 | 微 |
(2)物质D是NaOH.
16.李林同学参加中考体育加试,妈妈为他精心准备了以下食物:

从营养均衡角度来看,还缺少的营养素是( )

从营养均衡角度来看,还缺少的营养素是( )
| A. | 蛋白质 | B. | 糖类 | C. | 油脂 | D. | 维生素 |
13.如图是某反应的微观示意图.下列说法正确的是( )


| A. | 该反应属于置换反应 | B. | 反应前后分子种类没有发生变化 | ||
| C. | 反应后生成两种氧化物 | D. | 反应中乙和丁的质量比为32:44 |
20.在我们生活的物质世界里,不仅存在着形形色色的物质,而且物质还在不断地变化着.下列变化中,一定发生化学变化的是( )
| A. | 海水“晒盐” | B. | 煤的液化 | C. | 石油的分馏 | D. | 浓盐酸挥发 |
10. 硒被誉为“抗癌大王”.根据如图提供的硒的有关信息,下列说法中,正确的是( )
硒被誉为“抗癌大王”.根据如图提供的硒的有关信息,下列说法中,正确的是( )
 硒被誉为“抗癌大王”.根据如图提供的硒的有关信息,下列说法中,正确的是( )
硒被誉为“抗癌大王”.根据如图提供的硒的有关信息,下列说法中,正确的是( )| A. | 硒属于金属元素 | B. | 硒原子在化学反应中容易得到电子 | ||
| C. | 硒的原子结构示意图中x=4 | D. | 硒的相对原子质量是78.96 g |
 燃烧的条件可用如图所示火三角表示.
燃烧的条件可用如图所示火三角表示.