题目内容
12.某同学测得一瓶无色液体的 pH=3,将该溶液中滴加紫色石蕊试剂振荡,再加入过量的氢氧化钠溶液,颜色的变化是( )| A. | .红色变为蓝色 | B. | .红色变为紫色 | C. | 蓝色变为.红色 | D. | .紫色变为红色 |
分析 根据题意,某同学测得一瓶无色液体的pH=3,小于7,显酸性;将该溶液中滴加紫色石蕊试剂振荡,结合石蕊溶液遇酸性溶液变红色,遇碱性溶液变蓝色,结合酸碱发生中和反应,进行分析判断.
解答 解:某同学测得一瓶无色液体的pH=3,小于7,显酸性;将该溶液中滴加紫色石蕊试剂振荡,能使紫色石蕊溶液变红色,再加入过量的氢氧化钠溶液,酸性物质与过量的氢氧化钠溶液发生中和反应,最终溶液显碱性,能使紫色石蕊溶液变蓝色,故颜色的变化是红色变为蓝色.
故选:A.
点评 本题难度不大,掌握中和反应应用、溶液的酸碱性和溶液pH大小之间的关系等是正确解答本题的关键.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
2.人们在工作生活中为了防止事故,常采取一些安全措施.下列措施不安全的是( )
| A. | 到溶洞探险打火把照明 | |
| B. | 人居社区要配置消防设备和设置消防通道 | |
| C. | 夜晚发现液化气泄漏要立即开灯检查 | |
| D. | 严禁旅客携带易燃、易爆物品乘车 |
3.用氢氟酸对玻璃产品进行腐蚀雕刻的反应原理可表示为:SiO2+4HF═X↑+2H2O,则式中X的化学式为( )
| A. | SiF | B. | SiF4 | C. | SiH4 | D. | F4 |
17.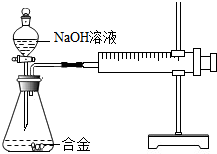 合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动.
合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动.
【提出问题】难道NaOH溶液也能与某些金属发生化学反应吗?
【查阅资料】
(1)铝能与氢氧化钠溶液反应,铁、铜不能与氢氧化钠溶液反应.
(2)铝与氢氧化钠溶液反应的化学方程式为:2AI+2NaOH+2H2O═2NaAIO2+3H2↑
(NaAlO2溶于水,溶液显无色)
进行猜想】猜想1:该合金粉末中除铝外,还含有铁
猜想2:该合金粉末中除铝外,还含有铜
猜想3:该合金粉末中除铝外,还含有铁、铜.
实验探究】下列实验(见表1)仅供选用的试剂:20%的硫酸溶液、30%的NaOH溶液.
表1实验记录
【得出结论】猜想3成立.
【反思】
1.一般来说,活泼金属能与稀硫酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.铝与稀硫酸发生化学反应的化学方程式是2Al+3H2SO4═Al2(SO4)3+3H2↑
2.上述实验中用到的稀硫酸由浓硫酸稀释得到,稀释浓硫酸的方法是:把浓硫酸沿烧杯壁慢慢注入水中,并不断搅拌.
3.若小明向合金粉末中加入的是足量的稀硫酸,则最终剩余的固体成分是铜.
拓展与分析】为了比较铝、铁、铜的金属活动性强弱,某同学设计一个实验方案,将金属铝和铜插入到硫酸亚铁溶液中其现象是铝表面有一层红色物质出现,铜表面无现象.,说明铝、铁、铜金属活动性由弱到强顺序是铝>铁>铜.
 合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动.
合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动.【提出问题】难道NaOH溶液也能与某些金属发生化学反应吗?
【查阅资料】
(1)铝能与氢氧化钠溶液反应,铁、铜不能与氢氧化钠溶液反应.
(2)铝与氢氧化钠溶液反应的化学方程式为:2AI+2NaOH+2H2O═2NaAIO2+3H2↑
(NaAlO2溶于水,溶液显无色)
进行猜想】猜想1:该合金粉末中除铝外,还含有铁
猜想2:该合金粉末中除铝外,还含有铜
猜想3:该合金粉末中除铝外,还含有铁、铜.
实验探究】下列实验(见表1)仅供选用的试剂:20%的硫酸溶液、30%的NaOH溶液.
表1实验记录
| 实验步骤 | 实验现象 | 结论 |
| ①取一定量的合金粉末,加过量的30%氢氧化钠溶液,充分反应后过滤,滤渣备用 | 粉末部分溶解,并有无色气体放出 | 合金中一定含有铝 |
| ②取步骤①所得滤渣,加过量20%的硫酸溶液,充分反应 | 滤渣部分溶解,并有无色气体放出,溶液呈浅绿色 | 合金中一定含有铁、铜 |
【反思】
1.一般来说,活泼金属能与稀硫酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.铝与稀硫酸发生化学反应的化学方程式是2Al+3H2SO4═Al2(SO4)3+3H2↑
2.上述实验中用到的稀硫酸由浓硫酸稀释得到,稀释浓硫酸的方法是:把浓硫酸沿烧杯壁慢慢注入水中,并不断搅拌.
3.若小明向合金粉末中加入的是足量的稀硫酸,则最终剩余的固体成分是铜.
拓展与分析】为了比较铝、铁、铜的金属活动性强弱,某同学设计一个实验方案,将金属铝和铜插入到硫酸亚铁溶液中其现象是铝表面有一层红色物质出现,铜表面无现象.,说明铝、铁、铜金属活动性由弱到强顺序是铝>铁>铜.
4. 在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如图所示的实验.
在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如图所示的实验.
(1)写出试管②中碳酸钠与氢氧化钙反应的化学方式:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究.
提出问题】滤液中除水外还含有哪些物质?
【猜想】小红认为:只含氢氧化钠;
小明认为:可能含有氢氧化钠、碳酸钠和氢氧化钙;
小亮认为:可能含有氢氧化钠和碳酸钠;
你认为还可能是可能含有氢氧化钠和氢氧化钙(写一种猜想).
【讨论】你认为小红、小明、小亮三位同学中谁的猜想不合理,请说明理由.小明猜想不合理;
因为Na2CO3和Ca(OH)2能发生反应,不能共存.
【实验设计】设计一个简单的实验证明你的猜想正确.
【实验分析】小亮同学针对自己的猜想进行了如下实验:
你认为小亮同学对实验结果判断是否正确?请说明理由不正确.因为氢氧化钠存在,滴入几滴稀盐酸量太少,不会立即出现气泡,但碳酸钠可能存在.
【反思拓展】
①在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑反应物是否有剩余.
②通过以上探究,你认为应怎样处理上述实验后的废液才能倒入下水道?在废液中加酸至溶液的pH=7.
 在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如图所示的实验.
在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等几位同学进行了如图所示的实验.(1)写出试管②中碳酸钠与氢氧化钙反应的化学方式:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(2)实验结束后,小红同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小红等几位同学对滤液的成分又进行了探究.
提出问题】滤液中除水外还含有哪些物质?
【猜想】小红认为:只含氢氧化钠;
小明认为:可能含有氢氧化钠、碳酸钠和氢氧化钙;
小亮认为:可能含有氢氧化钠和碳酸钠;
你认为还可能是可能含有氢氧化钠和氢氧化钙(写一种猜想).
【讨论】你认为小红、小明、小亮三位同学中谁的猜想不合理,请说明理由.小明猜想不合理;
因为Na2CO3和Ca(OH)2能发生反应,不能共存.
【实验设计】设计一个简单的实验证明你的猜想正确.
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,通入二氧化碳 | 白色沉淀 | 你的猜想正确 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气泡产生 | 自己的猜想不成立 |
【反思拓展】
①在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑反应物是否有剩余.
②通过以上探究,你认为应怎样处理上述实验后的废液才能倒入下水道?在废液中加酸至溶液的pH=7.
1.研究性学习小组测定实验室里一瓶久置的NaOH固体是否变质.
【提出问题】NaOH固体是否变质?
【猜想与假设】猜想1:没变质,全部是NaOH;
猜想2:全变质,全部是Na2CO3
猜想3:部分变质,既含有NaOH,又含有Na2CO3;
设计方案并进行实验】请你与他们一起完成,并回答所给问题.
上述步骤①中,滴加过量氯化钙溶液的目的是使样品中的Na2C03完全反应
【实验结论】通过实验,说明上述猜想中3是正确的.
【拓展】
要除去氢氧化钠中含有的碳酸钠,所用的方法(用化学方程式表示)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
【反思】通过探究,实验室中的氢氧化钠应密封保存.
【提出问题】NaOH固体是否变质?
【猜想与假设】猜想1:没变质,全部是NaOH;
猜想2:全变质,全部是Na2CO3
猜想3:部分变质,既含有NaOH,又含有Na2CO3;
设计方案并进行实验】请你与他们一起完成,并回答所给问题.
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述固体样品8g溶于100mL水配成溶液,向溶液中滴加 过量的氯化钙溶液充分反应后,静置. | 产生白色沉淀 | 说明久置固体中,一定含有Na2CO3 |
| ②用玻璃棒蘸取少量①中的上层清液滴在pH试纸上,与标准比色卡对比,测出pH | pH=10 | 说明固体中,还一定含有NaOH(填化学式). |
【实验结论】通过实验,说明上述猜想中3是正确的.
【拓展】
要除去氢氧化钠中含有的碳酸钠,所用的方法(用化学方程式表示)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
【反思】通过探究,实验室中的氢氧化钠应密封保存.
2.化学与健康息息相关.“APEC”会议的晚宴上有一道传统小吃“豌豆黄”,根据表格中的信息回答以下问题.
(1)“豌豆黄”中主要含有蛋白质、糖类和无机盐三类营养素.
(2)“豌豆黄”中含有钙元素.人体缺钙常会引起AC(填序号).
A.佝偻病 B.贫血症 C.骨质疏松 D.甲状腺肿大
(3)很多食物也能提供丰富的蛋白质.下列能提供丰富蛋白质的食品是B(填序号).

| 品名 | 豌豆黄 |
| 主要原料 | 豌豆 |
| 主要营养成分 | 蛋白质、糖类、钠、钙、钾、镁、铁等元素 |
(2)“豌豆黄”中含有钙元素.人体缺钙常会引起AC(填序号).
A.佝偻病 B.贫血症 C.骨质疏松 D.甲状腺肿大
(3)很多食物也能提供丰富的蛋白质.下列能提供丰富蛋白质的食品是B(填序号).

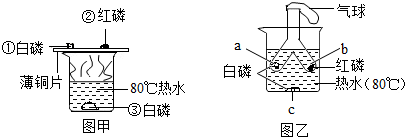
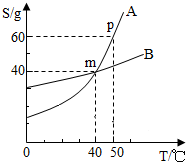 小明同学绘制了如图所示A、B两种固体物质的溶解度曲线:
小明同学绘制了如图所示A、B两种固体物质的溶解度曲线: