题目内容
5.工业上常用二氧化碳和氨气(化学式:NH3)反应来制取尿素[化学式:CO(NH2)2],该反应的化学方程式为:CO2+2NH3$\frac{\underline{\;\;\;催化剂\;\;\;}}{高温高压}$CO(NH2)2+H20,现生产240t尿素,需要氨气的质量为多少?分析 根据反应的化学方程式和尿素的质量可以计算反应的氨气质量.
解答 解:设需要氨气的质量为x,
CO2+2NH3$\frac{\underline{\;\;\;催化剂\;\;\;}}{高温高压}$CO(NH2)2+H20,
34 60
x 240t
$\frac{34}{x}$=$\frac{60}{240t}$,
x=136t,
答:需要氨气的质量是136t.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.如表是某同学对铁制品生锈情况的调查:
(1)从以上调查中,可知铁制品生锈的主要条件是与空气和氧气、水直接接触.
(2)下列保护铁资源的建议,不正确的是C(填序号).
A.防止铁制品腐蚀 B.回收利用废旧铁制品 C.任意开采铁矿石.
| 调查内容 | 掉漆的自行车 | 裸露在混凝土外的钢筋 | 涂油的无锈铁钉 | 镀铬的铁质剪刀 |
| 铁制品锈蚀的现象 | 风吹雨淋,时间长了,掉漆的部分会生锈 | 在潮湿的空气中,时间长了,裸露的钢筋表面会出现锈层 | 铁钉较长时间不生锈 | 剪刀较长时间 不生锈 |
(2)下列保护铁资源的建议,不正确的是C(填序号).
A.防止铁制品腐蚀 B.回收利用废旧铁制品 C.任意开采铁矿石.
5.下列化学实验基本操作中正确的是( )
| A. | 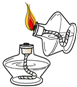 点燃酒精 | B. | 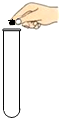 取用颗粒状固体 | C. | 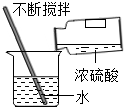 稀释浓硫酸 | D. |  给液体加热 |

 某化学实验小组欲探究稀盐酸、氢氧化钙的化学性质,取7支试管分别用A-G编号后,做如下实验(如图):
某化学实验小组欲探究稀盐酸、氢氧化钙的化学性质,取7支试管分别用A-G编号后,做如下实验(如图):