题目内容
10.请回答下列与CO2和CO有关的问题.(1)鉴别CO2和CO可用澄清的石灰水,写出有关反应的化学方程式Ca(OH)2+CO2=CaCO3↓+H2O;
(2)除去CO2中的CO可采用的方法是把混合气体通过灼热的CuO;
(3)CO2和CO化学性质不同的原因是分子构成.
分析 (1)根据二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水进行分析解答;
(2)根据一氧化碳和二氧化碳的化学性质的不同解答;
(3)根据分子的基本性质进行分析解答.
解答 解:
(1)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水进行,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O.
(2)根据一氧化碳和二氧化碳的化学性质,一氧化碳能与灼热的氧化铜反应生成铜和二氧化碳,二氧化碳不与氧化铜不反应,故可将混合气体通过灼热的氧化铜,既能除去一氧化碳又能增加二氧化碳,达到除去CO2中混有的少量CO的目的;
(3)CO和CO2都是碳的氧化物,但二者的化学性质不同,是因为它们分子的构成不同,不同种的分子性质不同.
故答案为:
(1)Ca(OH)2+CO2=CaCO3↓+H2O;
(2)把混合气体通过灼热的CuO;
(3)分子构成
点评 本题难度不大,掌握木炭和活性炭具有吸附性、分子的基本性质、二氧化碳的化学性质是正确解答本题的关键.

练习册系列答案
相关题目
1.下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
(1)上表中的两种物质在40℃时,KNO3的溶解度较大;
(2)将20℃KNO3的不饱和溶液转化为饱和溶液的方法有蒸发溶剂或降低温度和加KNO3;
(3)20℃时,将20gNaCl放入50g水中,所得溶液的质量是68gg;
(4)从NaCl溶液中得到NaCl晶体最好的放法是蒸发结晶.
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
(2)将20℃KNO3的不饱和溶液转化为饱和溶液的方法有蒸发溶剂或降低温度和加KNO3;
(3)20℃时,将20gNaCl放入50g水中,所得溶液的质量是68gg;
(4)从NaCl溶液中得到NaCl晶体最好的放法是蒸发结晶.
5.下列实验方案中,合理的是( )
| A. | 实验室制备CO2:用石灰石与稀硫酸反应 | |
| B. | 分离木炭粉和CuO:在空气中充分灼烧 | |
| C. | 检验氧化钙中是否有碳酸钙:加入足量的稀盐酸 | |
| D. | 除去盐酸中混有的H2SO4:加入适量的Ba(NO3)2溶液 |
2.下列事例属于化学变化的是( )
| A. | 生米煮成熟饭 | B. | 水变成水蒸气 | C. | 酒精挥发 | D. | 大石块打成粉末 |
19.下列说法正确的是( )
| A. | 非金属氧化物都能跟碱反应生成盐和水 | |
| B. | 固体物质的溶解度都随温度的升高而增大 | |
| C. | 常温下金属都为固态 | |
| D. | 置换反应一定有单质和化合物生成 |
20.下列盐中不能通过金属和盐发生置换反应而一步制得的是( )
| A. | AlCl3 | B. | FeCl3 | C. | ZnCl2 | D. | MgCl2 |

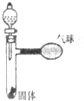 如图所示,打开分液漏斗,使其中的无色液体与试管中的面体接触反应,可观察到气球胀大现象,请分别写出一个符合图中现象和下要求的化学方程式:
如图所示,打开分液漏斗,使其中的无色液体与试管中的面体接触反应,可观察到气球胀大现象,请分别写出一个符合图中现象和下要求的化学方程式: