题目内容
化学探究小组取石灰石样品放在烧杯中,然后向其中加入一定量的稀盐酸,使之与样品充分反应(杂质不参加反应).测得生成二氧化碳气体的质量为4.4g.计算:样品中碳酸钙的质量是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据化学方程式利用二氧化碳的质量直接进行计算即可.
解答:解:设样品中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
=
解得:x=10g
答:样品中碳酸钙的质量为10g.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
| 100 |
| 44 |
| x |
| 4.4g |
解得:x=10g
答:样品中碳酸钙的质量为10g.
点评:本题直接根据化学方程式进行计算即可,很简单.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
全世界都在大力提倡“低碳生活”,下列做法不符合“低碳生活”的是( )
| A、鼓励私人购买家用轿车代替公交车 |
| B、积极开发新能源,减少使用化石燃料 |
| C、多种植物,保护植被 |
| D、节约用水,提倡水的二次使用 |
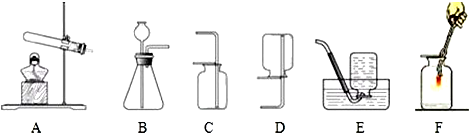
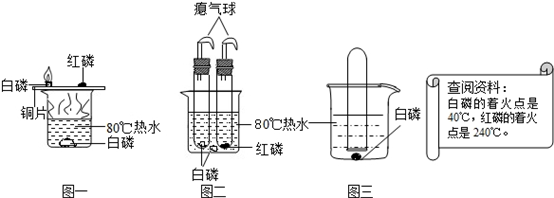
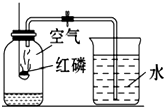 如图是空气中氧气含量测定实验的装置图,按要求回答问题
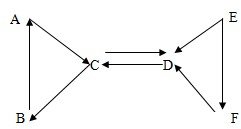
如图是空气中氧气含量测定实验的装置图,按要求回答问题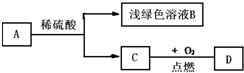 已知,A、B、C、D四种物质之间存在以下转化关系.其中C是单质,D是相对分子质量最小的氧化物.试回答
已知,A、B、C、D四种物质之间存在以下转化关系.其中C是单质,D是相对分子质量最小的氧化物.试回答