题目内容
18.把4g硫粉放在一定质量的氧气中燃烧,有关实验数据如表所示.请计算第三次实验中,生成SO2的质量是多少?请列出方程写出必要的计算过程.| 第一次 | 第二次 | 第三次 | |
| O2的质量 | 3 | 4 | 6 |
| SO2的质量 | 6 |
分析 根据硫在氧气中燃烧的化学方程式及各物质之间的质量关系,第三次氧气过量,根据硫的质量计算二氧化硫的质量.
解答 解:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2,硫、氧气、二氧化硫的质量比为:32::32:64=1:1:2,故第三次氧气过量,
设生成SO2的质量是x
S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2
32 64
4g x
$\frac{32}{64}=\frac{4g}{x}$
x=8g
答:生成SO2的质量是8g.
点评 本题主要考查学生运用化学方程式和质量守恒定律综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
8.下列变化要消耗空气中氧气的是( )
| A. | 干冰在空气中升华 | B. | 钢铁在空气中生锈 | ||
| C. | 生石灰在空气中变质 | D. | 澄清石灰水在空气中变浑浊 |
9.(1)计算下列常见氮肥的相对分子质量或氮元素的质量的分数.
(2)用氨气与二氧化碳反应生成尿素的化学方程式为2NH3+CO2=CO(NH2)2+H2O,现要生产120kg尿素,需要氨气多少千克?
| 常见氮肥 | NH4NO3 | NH4HCO3 | CO(NH2)2 |
| 相对分子质量 | 80 | ① | 60 |
| 氮元素质量分数 | 35% | 17.7% | ② |
13.下列生活现象中属于物理变化的是( )
| A. | 呼吸作用 | B. | 用粮食酿酒 | C. | 食物腐烂 | D. | 木炭吸附 |
13.下列变化中前者是物理变化,后者是化学变化的是( )
| A. | 牛奶变酸,蜡烛燃烧 | B. | 瓷器破碎,水分蒸发 | ||
| C. | 冰块降温,铜器变绿 | D. | 铁生锈,空气液化 |
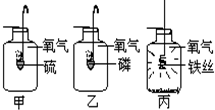 甲、乙、丙是三个实验的示意图,试回答下列问题:发生的三个反应有多个共同的特点,请写出其中三点:
甲、乙、丙是三个实验的示意图,试回答下列问题:发生的三个反应有多个共同的特点,请写出其中三点: