题目内容
著名的科学家诺贝尔经过长期的试验,研制出安全炸药.炸药三硝酸甘油酯(C3H5N3O9)发生爆炸的化学方程式:4C3H5N3O9
 12CO2↑+10H2O↑+6X↑+O2↑
12CO2↑+10H2O↑+6X↑+O2↑(1)推断X的化学式为______.
(2)炸药三硝酸甘油酯的相对分子量是______,其中化学式中氮元素的质量分数是______.
【答案】分析:(1)根据质量守恒定律的微观解释:化学反应前后原子的种类和数目不变.可知在化学反应方程式中,反应物和生成物中所含的原子的种类和数目相同.由此可推断化学反应方程式中反应物或生成物的化学式.
(2)C3H5N3O9的相对分子质量=(碳的相对原子质量×碳原子个数)+(氢的相对原子质量×氢原子个数)+(氮的相对原子质量×氮原子个数)+(氧的相对原子质量×氧原子个数).
解答:解:(1)根据质量守恒定律和化学方程式可得,X的化学式中应含有碳原子的个数为:(4×3-12)÷6=0,应含有氢原子的个数为:(4×5-10×2)÷6=0,应含有氮原子的个数为:(4×3)÷6=2,应含有氧原子的个数为:(4×9-12×2-10-2)÷6=0.故可判断,X的化学式为:N2.
(2)C3H5N3O9的相对分子质量=12×3+1×5+14×3+16×9=227;氮元素的质量分数是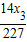 ×100%=18.5%.
×100%=18.5%.
故答案为:(1)N2;(2)227;18.5%.
点评:本题主要考查学生运用化学式和质量守恒定律进行分析推断和计算的能力.
(2)C3H5N3O9的相对分子质量=(碳的相对原子质量×碳原子个数)+(氢的相对原子质量×氢原子个数)+(氮的相对原子质量×氮原子个数)+(氧的相对原子质量×氧原子个数).
解答:解:(1)根据质量守恒定律和化学方程式可得,X的化学式中应含有碳原子的个数为:(4×3-12)÷6=0,应含有氢原子的个数为:(4×5-10×2)÷6=0,应含有氮原子的个数为:(4×3)÷6=2,应含有氧原子的个数为:(4×9-12×2-10-2)÷6=0.故可判断,X的化学式为:N2.
(2)C3H5N3O9的相对分子质量=12×3+1×5+14×3+16×9=227;氮元素的质量分数是
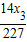 ×100%=18.5%.
×100%=18.5%.故答案为:(1)N2;(2)227;18.5%.
点评:本题主要考查学生运用化学式和质量守恒定律进行分析推断和计算的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目