题目内容
硅及其氧化物能发生如下反应:
①Si+O2
SiO2
②Si+2NaOH+H2O→Na2SiO3+2H2↑
③SiO2+2C
Si+2CO
④SiO2+Na2CO3
Na2SiO3+CO2↑
下列说法错误的是( )
①Si+O2
| △ |
②Si+2NaOH+H2O→Na2SiO3+2H2↑
③SiO2+2C
| 高温 |
④SiO2+Na2CO3
| 高温 |
下列说法错误的是( )
| A、①属于化合反应 |
| B、Na2SiO3中Si元素的化合价为+4价 |
| C、反应③中氧化剂是C |
| D、Si和SiO2可以相互转化 |
考点:反应类型的判定,有关元素化合价的计算,书写化学方程式、文字表达式、电离方程式
专题:结合课本知识的信息
分析:A、根据反应物及生成物的特点判断反应类型;
B、根据化合物中正负化合价的代数和为零,分析硅元素的化合价;
C、根据失氧的是氧化剂分析;
D、根据硅和二氧化硅的化学性质分析.
B、根据化合物中正负化合价的代数和为零,分析硅元素的化合价;
C、根据失氧的是氧化剂分析;
D、根据硅和二氧化硅的化学性质分析.
解答:解:A、①的反应物是两种,生成物是一种,属于化合反应,故A说法正确;
B、Na2SiO3中钠元素的化合价为+1价,氧元素为-2价,根据正负化合价的代数和为0可知Si的化合价为+4价,故B说法正确;
C、二氧化硅在反应中失氧,是氧化剂,C在反应中夺氧,是还原剂,故C说法错误;
D、Si和氧气在加热条件下会生成二氧化硅,SiO2和碳在高温条件下会生成硅,故两者在一定条件下可以相互转化,故D说法正确.
故选:C.
B、Na2SiO3中钠元素的化合价为+1价,氧元素为-2价,根据正负化合价的代数和为0可知Si的化合价为+4价,故B说法正确;
C、二氧化硅在反应中失氧,是氧化剂,C在反应中夺氧,是还原剂,故C说法错误;
D、Si和氧气在加热条件下会生成二氧化硅,SiO2和碳在高温条件下会生成硅,故两者在一定条件下可以相互转化,故D说法正确.
故选:C.
点评:本题考查的知识点较多,可以从化学方程式中的反应物和生成物的种类、条件方面进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
下列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
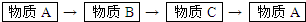
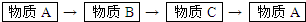
| A、Fe→Fe2O3→FeSO4→Fe |
| B、CO→CO2→H2CO3→CO |
| C、H2SO4→Na2SO4→NaNO3→H2SO4 |
| D、HCl→CuCl2→BaCl2→HCl |
互为同素异形体的一组物质是( )
| A、氧气与液氧 | B、水银与银 |
| C、干冰与冰 | D、金刚石与石墨 |
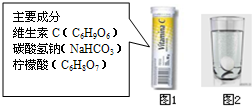 某研究小组发现,维C泡腾片(保健药品,见图1)溶于水时,有许多气泡产生(如图2).该小组同学进行如下探究.
某研究小组发现,维C泡腾片(保健药品,见图1)溶于水时,有许多气泡产生(如图2).该小组同学进行如下探究.