题目内容
为测定氯化钠和碳酸钠固体混合物中氯化钠的质量分数,有以下两个实验方案:
(1)方案1:
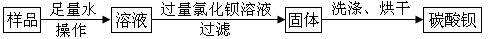
请问:①操作的名称是 。要计算样品中氯化钠的质量分数,实验中必须测量的数据是:碳酸钡的质量和 ;
②若过滤所得固体未经洗涤即烘干称量,测得样品中氯化钠的质量分数将 。(填“偏大”、“偏低”或“不变”)
(2)方案2:通过测定样品和足量硫酸溶液反应产生气体的质量来计算样品中氯化钠的质量分数。若测得各物质的质量(g):样品质量为a,所用硫酸溶液质量为b,完全反应后混合溶液质量为c,则生成气体的质量为 g。(用a、b、c表示)
【答案】
① 溶解 样品质量 ② 偏低 (2)a+b-c
【解析】(1)方案1:①操作是将固体溶液水,名称是溶解;因为最终要求质量分数,因此缺少样品的质量。②过滤所得固体是碳酸钡,未经洗涤即烘干称量会使得质量增大,通过计算碳酸钠的质量也会增大,从而氯化钠的质量就相应地减少,最终使氯化钠的质量分数减小。
(2)方案2,根据反应前后物质的总质量不变来解答,反应所有的总质量为:a+b,反应结束后,总质量应该是混合溶液的质量与生成的气体的质量的和,故生成气体的质量为a+b-c

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目




