题目内容
19.某厂生产的加钙食盐含有的成分为氯化钠和碳酸钙,请计算:为了测定此食盐中的碳酸钙的质量分数,取20g这种食盐,加入足量的100g稀盐酸中(已知氯化钠不与稀盐酸反应),充分反应后,称量剩余物质质量为119.78g(1)生成CO2质量为0.22g
(2)请计算此加钙食盐中碳酸钙的质量分数.(要求写出计算过程)
分析 (1)根据质量守恒定律可知,碳酸钙和盐酸生成氯化钙、水和二氧化碳,所以反应前后质量减少的就是生成二氧化碳的质量进行解答;
(2)根据二氧化碳的质量即可计算出参与反应的碳酸钙的质量(即20g这种盐中碳酸钙的质量);然后再计算出此加钙食盐中碳酸钙的质量分数.
解答 解:(1)根据质量守恒定律可知,生成CO2质量=20g+100g-119.78g=0.22g;
(2)设参与反应的碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 0.22g
$\frac{100}{x}$=$\frac{44}{0.22g}$
x=0.5g
此加钙食盐中碳酸钙的质量分数为:$\frac{0.5g}{20g}$×100%=2.5%.
答:此加钙食盐中碳酸钙的质量分数为2.5%.
故答案为:(1)0.22g;
(2)2.5%.
点评 本题考查了根据化学方程式进行的有关计算,完成此题,可以依据化学方程式的有关基础计算进行.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
7.锌和过量浓硫酸在加热的条件下会产生一种有刺激性气味的气体,经实验证实该气体为SO2,同时还有白色沉淀物产生,将反应后的混合物加入到一定量的水中,白色沉淀物会逐渐溶解.下列说法正确的( )
| A. | 该反应为置换反应 | |
| B. | 物质的浓度不会影响物质的化学性质 | |
| C. | 自色沉淀物可能是硫酸锌晶体 | |
| D. | 若在白色沉淀物溶解后的溶液中继续加锌粒,无气体产生 |
4.如图所示的实验操作不正确的是( )
| A. | 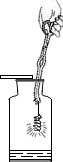 铁丝在氧气中燃烧 | B. | 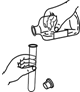 倾倒液体 | ||
| C. | 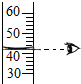 读取液体的体积 | D. | 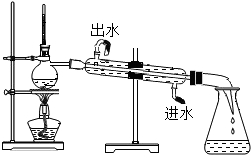 制取蒸馏水 |
11. 如图是一组物质发生化学反应的微观示意图,其中“
如图是一组物质发生化学反应的微观示意图,其中“ ”、“
”、“ ”、“
”、“ ”分别表示A、B、C三种不同的原子.下列说法正确的是( )
”分别表示A、B、C三种不同的原子.下列说法正确的是( )
 如图是一组物质发生化学反应的微观示意图,其中“
如图是一组物质发生化学反应的微观示意图,其中“ ”、“
”、“ ”、“
”、“ ”分别表示A、B、C三种不同的原子.下列说法正确的是( )
”分别表示A、B、C三种不同的原子.下列说法正确的是( )| A. | 该反应中有2种化合物 | |
| B. | 该反应属于分解反应 | |
| C. | B2一定是催化剂 | |
| D. | 该反应的化学方程式可能为2AC3+B2=A2+3C2+B2 |
8.下列实验操作和分析都正确的是B.
| 操 作 | 分 析 | |
| A | 用带火星的木条伸入集气瓶底部来检验CO2是否收集满 | 因为CO2的密度比空气大 |
| B | 木炭还原氧化铜时,加热用的酒精灯可加网罩,最好使用酒精喷灯 | 网罩的作用是使火焰集中并提高温度 |
| C | 测空气中氧气含量时,要加入过量的红磷 | 红磷过量的目的是使实验现象明显 |
| D | 取一小块乒乓球碎片和滤纸碎片,分别用坩埚钳夹住放在酒精灯火焰上加热 | 目的是证明这两种物质都是可燃物 |
1.下列对某一主题的知识归纳,正确的一组是( )
| A有关判断 | B能源与资源 |
| 水和冰的共存物----是纯净物也是氧化物 木材燃烧质量减小----符合质量守恒定律 | 天然气、可燃冰----主要成分都是CH4,是较清洁的燃料 焦炉煤气----煤干馏的产物,燃烧不会产生二氧化碳 |
| C燃烧与灭火 | D化学与生活 |
| 白磷易自然而红磷不易----着火点不同 吹灭蜡烛----降低蜡烛着火点 | 食醋----铁锅做饭时,加食醋可为人体补铁 钢----只含金属元素 |
| A. | A | B. | B | C. | C | D. | D |

 兴趣小组欲测定某未知浓度Ba(OH)2溶液的溶质质量分数,请你和他们一起完成实验并回答有关问题.
兴趣小组欲测定某未知浓度Ba(OH)2溶液的溶质质量分数,请你和他们一起完成实验并回答有关问题.