题目内容
 (2012?朝阳区一模)以下为初中化学常见物质,由H、C、O、Cl、Na、Ca、Cu、Fe中的元素组成.
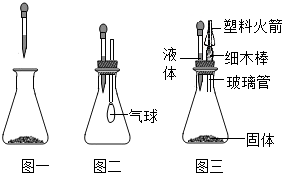
(2012?朝阳区一模)以下为初中化学常见物质,由H、C、O、Cl、Na、Ca、Cu、Fe中的元素组成.(1)利用图一进行实验
①若B为不溶水的白色粉末,将A溶液滴入后产生气泡,则B的化学式 为
CaCO3
CaCO3
;②若将A溶液滴入到C粉末中,观察到溶液变为黄色,则反应的化学方程式为
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+6HCl=2FeCl3+3H2O
;③若将蓝色D溶液滴入到E粉末中,可观察到溶液变为浅绿色,则反应的化学方程式为
Fe+CuCl2=Cu+FeCl2
Fe+CuCl2=Cu+FeCl2
;(2)利用图二进行实验
挤压胶头滴管将F溶液滴入到盛有H的锥形瓶中,可观察到气球胀大,得到K溶液,K溶液可继续与H反应生成M,其中K与M含有相同的金属元素,则该反应的化学方程式为
Na2CO3+H2O+CO2═2NaHCO3
Na2CO3+H2O+CO2═2NaHCO3
;(3)利用图三进行实验--“发射火箭”表演时,挤压胶头滴管,套着塑料火箭的轻质细木棒向上冲出,完成发射.则锥形瓶中的固体和胶头滴管中的液体可能是上述物质中的:
| 序号 物质 |
① | ② | ③ | ④ | ⑤ |
| 液体 | |||||
| 固体 |
分析:根据题干提供的信息进行分析,(1)①B为不溶水的白色粉末,将A溶液滴入后产生气泡,则是碳酸盐遇酸的反应,故B可能为碳酸钙,A为盐酸;
②将A溶液滴入到C粉末中,观察到溶液变为黄色,则C是氧化铁;
③将蓝色D溶液滴入到E粉末中,可观察到溶液变为浅绿色,则蓝色溶液D为氯化铜,E为铁;
(2)将F溶液滴入到盛有H的锥形瓶中,可观察到气球胀大,得到K溶液,则是反应消耗了气体,使瓶内的压强减小,可能是氢氧化钠与二氧化碳的反应,生成碳酸钠和水,碳酸钠能继续与二氧化碳反应生成碳酸氢钠.
②将A溶液滴入到C粉末中,观察到溶液变为黄色,则C是氧化铁;
③将蓝色D溶液滴入到E粉末中,可观察到溶液变为浅绿色,则蓝色溶液D为氯化铜,E为铁;
(2)将F溶液滴入到盛有H的锥形瓶中,可观察到气球胀大,得到K溶液,则是反应消耗了气体,使瓶内的压强减小,可能是氢氧化钠与二氧化碳的反应,生成碳酸钠和水,碳酸钠能继续与二氧化碳反应生成碳酸氢钠.
解答:解:(1)①B为不溶水的白色粉末,将A溶液滴入后产生气泡,则是碳酸盐遇酸的反应,故B可能为碳酸钙,A为盐酸,故填:CaCO3;
②将A溶液滴入到C粉末中,观察到溶液变为黄色,则C是氧化铁,氧化铁能与盐酸反应生成氯化铁和水,故填:Fe2O3+6HCl=2FeCl3+3H2O;
③将蓝色D溶液滴入到E粉末中,可观察到溶液变为浅绿色,则蓝色溶液D为氯化铜,E为铁,铁能与氯化铜反应生成铜和氯化亚铁,故填:Fe+CuCl2=Cu+FeCl2
(2)将F溶液滴入到盛有H的锥形瓶中,可观察到气球胀大,得到K溶液,则是反应消耗了气体,使瓶内的压强减小,可能是氢氧化钠与二氧化碳的反应,生成碳酸钠和水,碳酸钠能继续与二氧化碳反应生成碳酸氢钠,故填:Na2CO3+H2O+CO2
═2NaHCO3;
(3)挤压胶头滴管,套着塑料火箭的轻质细木棒向上冲出,完成发射.则锥形瓶中的固体和胶头滴管中的液体反应能生成气体或放出大量的热,从而导致锥形瓶内的压强增大,可以是盐酸与碳酸钠、碳酸钙、碳酸氢钠、铁的反应,这些反应有气体放出,也可以是盐酸与氢氧化钠固体的反应,此反应中氢氧化钠固体溶于水以及氢氧化钠和盐酸的反应都会放出热量,使温度升高,从而锥形瓶中的压强增大,故填:
②将A溶液滴入到C粉末中,观察到溶液变为黄色,则C是氧化铁,氧化铁能与盐酸反应生成氯化铁和水,故填:Fe2O3+6HCl=2FeCl3+3H2O;
③将蓝色D溶液滴入到E粉末中,可观察到溶液变为浅绿色,则蓝色溶液D为氯化铜,E为铁,铁能与氯化铜反应生成铜和氯化亚铁,故填:Fe+CuCl2=Cu+FeCl2
(2)将F溶液滴入到盛有H的锥形瓶中,可观察到气球胀大,得到K溶液,则是反应消耗了气体,使瓶内的压强减小,可能是氢氧化钠与二氧化碳的反应,生成碳酸钠和水,碳酸钠能继续与二氧化碳反应生成碳酸氢钠,故填:Na2CO3+H2O+CO2
═2NaHCO3;
(3)挤压胶头滴管,套着塑料火箭的轻质细木棒向上冲出,完成发射.则锥形瓶中的固体和胶头滴管中的液体反应能生成气体或放出大量的热,从而导致锥形瓶内的压强增大,可以是盐酸与碳酸钠、碳酸钙、碳酸氢钠、铁的反应,这些反应有气体放出,也可以是盐酸与氢氧化钠固体的反应,此反应中氢氧化钠固体溶于水以及氢氧化钠和盐酸的反应都会放出热量,使温度升高,从而锥形瓶中的压强增大,故填:
| 序号 物质 |
① | ② | ③ | ④ | ⑤ |
| 液体 | HCl | HCl | HCl | HCl | HCl |
| 固体 | NaHCO3 | Na2CO3 | CaCO3 | Fe | NaOH |
点评:本题考查了常见物质的性质,以及有关物质成分的推断,完成此题,可以依据题干提供的信息结合物质的性质进行.

练习册系列答案
相关题目

