题目内容
如图中的A~I表示几种初中化学常见的物质,其中A、D、I氧化物,I中两种元素质量之比为3:4;B元素在地壳中的含量位居第三;C由三种元素组成;G为紫红色.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.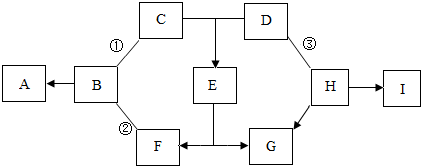
(1)写出G的化学式 ;H的化学式 .
(2)反应①、②和③的基本反应类型相同,该基本反应类型是 .
(3)B→A反应的化学方程式 .
(4)C与D反应的化学方程式为 .

(1)写出G的化学式
(2)反应①、②和③的基本反应类型相同,该基本反应类型是
(3)B→A反应的化学方程式
(4)C与D反应的化学方程式为
考点:物质的鉴别、推断,化学式的书写及意义,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:框图型推断题
分析:本题的突破口是B元素在地壳中的含量位居第三,因此是铝,而B能够转化成A氧化物,因此A是氧化铝;铝还能和C和F反应,因此C和F是酸和盐,C由三种元素组成且能够和D氧化物反应,因此确定C是硫酸,E是盐溶液;F是盐且是排在铝后面的金属形成的盐溶液;G是紫红色的铜,所以E硫酸铜,则D为氧化铜;H能够和氧化铜反应,说明H具有还原性,而I是氧化物,I中两种元素质量之比为3:4,且I是H反应产生的,所以I为一氧化碳,然后带入验证回答问题即可.
解答:解:B元素在地壳中的含量位居第三,因此是铝,而B能够转化成A氧化物,因此A是氧化铝;铝还能和C和F反应,因此C和F是酸和盐,C由三种元素组成且能够和D氧化物反应,因此确定C是硫酸,E是硫酸盐,F是盐且是排在铝后面的金属形成的盐溶液,如硫酸亚铁;G是紫红色的铜,所以E硫酸铜,则D为氧化铜;H能够和氧化铜反应,说明H具有还原性,而I是氧化物,I中两种元素质量之比为3:4,且I是H反应产生的,所以I为一氧化碳,H是碳.
(1)G为紫红色的铜,H的化学式C;故答案为:Cu; C;
(2)反应①是硫酸和铝的反应、②是铝和硫酸盐的反应;③是碳和氧化铜的反应,三个反应都是置换反应;故答案为:置换反应;
(3)B是铝,A是氧化铝,因此B→A反应的化学方程式为:4Al+3O2
2Al2O3;故答案为:4Al+3O2
2Al2O3;
(4)C与D反应,即为硫酸与氧化铜的化学方程式为CuO+H2SO4═CuSO4+H2O
故答案为:
(1)Cu; C; (2)置换反应;(3)4Al+3O2
2Al2O3; (4)CuO+H2SO4═CuSO4+H2O
(1)G为紫红色的铜,H的化学式C;故答案为:Cu; C;
(2)反应①是硫酸和铝的反应、②是铝和硫酸盐的反应;③是碳和氧化铜的反应,三个反应都是置换反应;故答案为:置换反应;
(3)B是铝,A是氧化铝,因此B→A反应的化学方程式为:4Al+3O2
| ||
| ||
(4)C与D反应,即为硫酸与氧化铜的化学方程式为CuO+H2SO4═CuSO4+H2O
故答案为:
(1)Cu; C; (2)置换反应;(3)4Al+3O2
| ||
点评:本题是一个根据常见物质的性质展开的推断题,解决本类题目的关键是找准解题的突破口,然后利用物质的性质正推、逆推、交叉推等途径得出结论,最后带入验证即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
属于结晶水合物的是( )
| A、食盐 | B、硝酸钾 |
| C、硝酸钠 | D、胆矾 |
下列物质的应用不发生化学变化的是( )
①在食品袋内充氮气防腐②用二氧化碳灭火③氧气用于气焊④用燃烧的蜡烛照明.
①在食品袋内充氮气防腐②用二氧化碳灭火③氧气用于气焊④用燃烧的蜡烛照明.
| A、①② | B、③④ |
| C、①③④ | D、①②③ |
 如图两圆相交部分是五种物质中两两之间相互反应的示意图.下列对反应现象的说法中,错误的是( )
如图两圆相交部分是五种物质中两两之间相互反应的示意图.下列对反应现象的说法中,错误的是( )| A、a处形成浅绿色溶液 |
| B、b处形成大量气泡 |
| C、c处反应生成氯化钠 |
| D、d处溶液呈红色 |