题目内容
11.如图为元素周期表中某一周期元素的原子结构示意图,请回答下列问题.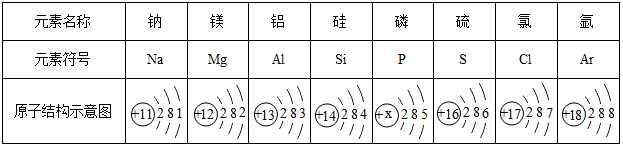
(1)表中磷原子的核内质子数x=15;
(2)表中具有相对稳定结构的元素是Ar;
(3)镁元素与氯元素形成的化合物化学式为MgCl2;
(4)上述元素在周期表中处于同一周期的原因是电子层数相同.
分析 (1)根据元素周期律:同周期元素从左到右质子数或原子序数依次递增;进行解答;
(2)最外层具有8个电子的原子具有相对稳定结构;
(3)根据化合物的化学式的写法来分析;
(4)根据元素周期数与电子层数的关系进行分析解答.
解答 解:(1)根据元素周期律:同周期元素从左到右质子数或原子序数依次递增;因此表中磷原子的质子数x=15;故答案为:15;
(2)最外层具有8个电子的原子具有相对稳定结构,表中具有相对稳定结构的元素氩元素.故填:Ar;
(3)镁元素显+2价,氯元素显-1价,二者组成的化合物的化学式为MgCl2;故填:MgCl2;
(4)由元素周期表中某一周期元素的原子结构示意图可以看出,处于同一周期的原子,核外电子层数相同.故填:电子层数相同.
点评 本题难度不大,是常考的题型,掌握同一周期的各原子结构示意图的特点、化学式的书写等是正确解答此类题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.如图是三种微粒的结构示意图,有关它们的说法正确的是( )


| A. | 它们都是原子 | B. | 它们的核外电子层不同 | ||
| C. | 它们属于同种元素的微粒 | D. | 它们都具有稳定的结构 |
16.燃烧、缓慢氧化、自燃的共同点是( )
| A. | 都属于化合反应 | B. | 都发光 | C. | 都属于氧化反应 | D. | 都属于分解反应 |
3.下列化合物中含有+7价的元素是( )
| A. | KClO3 | B. | KClO | C. | H2SO4 | D. | HClO4 |
1.不显电性的一组粒子是( )
| A. | 中子,原子,分子 | B. | 质子,中子,电子 | ||
| C. | 原子核,原子,分子 | D. | 中子,电子,原子 |
