题目内容
19.已知镁能与空气中氮气反应,化学方程式为:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2,若有1.00克镁在空气中充分燃烧,生成物的质量一定不可能的是( )| A. | 1.20~1.35克 | B. | 1.42~1.62克 | C. | 1.55~1.65克 | D. | 1.42~1.55克 |
分析 求出1克的镁在氧气中完全燃烧生成物的质量,再求出1克镁在氮气完全燃烧生成物的质量,则镁在空气中燃烧生成物的质量就在这两个质量之间.
解答 解:设12克镁在氧气中完全燃烧生成物的质量为x
2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO
48 80
1g x
$\frac{48}{80}=\frac{1g}{x}$
x=1.67g
设1克镁在氮气在完全燃烧生成物的质量为y
3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2
72 100
1g y
$\frac{72}{100}=\frac{1g}{y}$
y=1.39g
12克镁在空气在燃烧生成物的质量范围为大于1.39g,小于1.67克,故A不在范围,故选A.
点评 本题中生成物的质量我们并不能算出一个准确的值,只能计算出一个范围,该范围内的质量都有可能是生成物的质量.

练习册系列答案
相关题目
7.下列化学用语中,数字“2”的说法正确的是( )
①2H ②2NH3 ③SO2 ④H2O ⑤Mg2+ ⑥2OH- ⑦${\;}_{CuO}^{+2}$.
①2H ②2NH3 ③SO2 ④H2O ⑤Mg2+ ⑥2OH- ⑦${\;}_{CuO}^{+2}$.
| A. | 表示分子个数的是①② | B. | 表示分子中原子个数的是③④ | ||
| C. | 表示离子个数的是⑤⑥ | D. | 表示离子所带电荷数的是⑤⑦ |
14.关于分子、原子、离子的描述中,不正确的是( )
| A. | 原子可以构成分子,也可以形成离子 | |
| B. | 原子种类由核内质子数决定,原子的化学性质主要由最外层电子数决定 | |
| C. | 它们都可以直接构成物质 | |
| D. | 原子中的原子核一定由质子和中子构成 |
4.“绿色化学”是当今社会提出的一个新概念,杜绝污染源,提高原子的利用率是“绿色化学”的重要,衡量指标.下列物质均可做氧化剂①O3;②KMnO4;③浓H2SO4;④H2O2;⑤浓HNO3;⑥Ca(ClO)2;⑦KCr2O7其中可称为绿色氧化剂的是( )
| A. | ①④ | B. | ③⑤ | C. | ①②⑥⑦ | D. | ②⑦ |
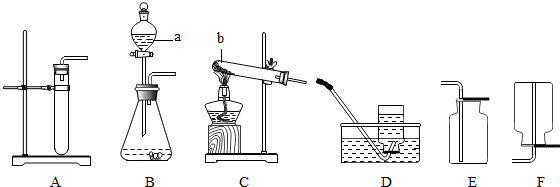
11.如图图象与所属实验现象相符的是( )
| A. | 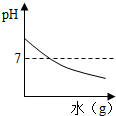 稀释NaOH溶液 | B. |  镁在空气中燃烧 | C. | 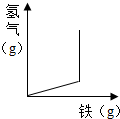 铁加入稀盐酸中 | D. | 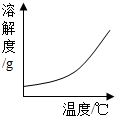 氧气的溶解度 |
8.为测定某三氧化钨样品中三氧化钨的质量分数,采用如图所示装置进行实验.
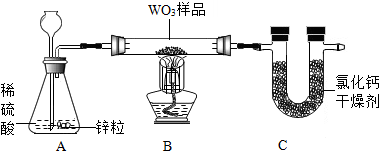
已知,该实验中三氧化钨样品的质量为13.0g,样品中的杂质不参加反应,WO3反应完全,化学方程式为:WO3+3H2$\frac{\underline{\;高温\;}}{\;}$W+3H2O,U形管C中干燥剂足量.吸收完全.该小组经过规范的实验操作后得到的数据如表.
(1)A中反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑.
(2)选择装置的实验数据计算样品中WO3的B质量分数较可靠.
(3)计算样品中WO3的质量分数(精确到0.1%),写出必要的计算过程.(可能用到的相对原子质量:H.一l O-16 W-184)

已知,该实验中三氧化钨样品的质量为13.0g,样品中的杂质不参加反应,WO3反应完全,化学方程式为:WO3+3H2$\frac{\underline{\;高温\;}}{\;}$W+3H2O,U形管C中干燥剂足量.吸收完全.该小组经过规范的实验操作后得到的数据如表.
| 实验前 | 实验后 | |
| B装置的质量(克) | 45.5 | 43.1 |
| C装置的质量(克) | 100.5 | 103.3 |
(2)选择装置的实验数据计算样品中WO3的B质量分数较可靠.
(3)计算样品中WO3的质量分数(精确到0.1%),写出必要的计算过程.(可能用到的相对原子质量:H.一l O-16 W-184)