题目内容
按要求用化学符号或化学符号表示的意义
①二个亚铁离子 ; ②负二价的硫元素 ;③地壳中含量最多的元素和含量最多的金属元素组成的化合物的化学式 ④硫酸铝 ⑤碳酸钠 ⑥两个硫酸根离子 ; ⑦2N2 ;⑧氦气 .
①二个亚铁离子
考点:化学符号及其周围数字的意义,化学式的书写及意义
专题:化学用语和质量守恒定律
分析:离子带的电荷数应该标在元素符号的右上角;
元素的化合价应该标在元素符号的正上方;
地壳中含量最多的元素是氧元素,含量最多的金属元素是铝元素,氧元素和铝元素组成的化合物是氧化铝,氧化铝中,铝元素的化合价是+3,氧元素的化合价是-2,根据化合物中元素化合价代数和为零可知,氧化铝中铝原子和氧原子的个数比是2:3;
硫酸铝中,铝元素的化合价是+3,硫酸根的化合价是-2,根据化合物中元素化合价代数和为零可知,硫酸铝中铝原子和硫酸根的个数比是2:3;
碳酸钠中,钠元素的化合价是+1,碳酸根的化合价是-2,根据化合物中元素化合价代数和为零可知,碳酸钠中钠原子额碳酸根的个数比是2:1;
每个硫酸根离子带2个单位负电荷;
氮气的化学式前面加上相应的数字表示氮分子的个数;
稀有气体都是单原子构成的分子.
元素的化合价应该标在元素符号的正上方;
地壳中含量最多的元素是氧元素,含量最多的金属元素是铝元素,氧元素和铝元素组成的化合物是氧化铝,氧化铝中,铝元素的化合价是+3,氧元素的化合价是-2,根据化合物中元素化合价代数和为零可知,氧化铝中铝原子和氧原子的个数比是2:3;
硫酸铝中,铝元素的化合价是+3,硫酸根的化合价是-2,根据化合物中元素化合价代数和为零可知,硫酸铝中铝原子和硫酸根的个数比是2:3;
碳酸钠中,钠元素的化合价是+1,碳酸根的化合价是-2,根据化合物中元素化合价代数和为零可知,碳酸钠中钠原子额碳酸根的个数比是2:1;
每个硫酸根离子带2个单位负电荷;
氮气的化学式前面加上相应的数字表示氮分子的个数;
稀有气体都是单原子构成的分子.
解答:解:①二个亚铁离子可以表示为2Fe2+;
②负二价的硫元素可以表示为
;
③地壳中含量最多的元素和含量最多的金属元素组成的化合物是氧化铝,氧化铝的化学式是Al2O3;
④硫酸铝可以表示为Al2(SO4)3;
⑤碳酸钠可以表示为Na2CO3;
⑥两个硫酸根离子可以表示为2SO42-;
⑦2N2表示2个氮分子;
⑧氦气可以表示为He.
故填:2Fe2+;
;Al2O3;Al2(SO4)3;Na2CO3;2SO42-; 2个氮分子;He.
②负二价的硫元素可以表示为
| -2 |
| S |
③地壳中含量最多的元素和含量最多的金属元素组成的化合物是氧化铝,氧化铝的化学式是Al2O3;
④硫酸铝可以表示为Al2(SO4)3;
⑤碳酸钠可以表示为Na2CO3;
⑥两个硫酸根离子可以表示为2SO42-;
⑦2N2表示2个氮分子;
⑧氦气可以表示为He.
故填:2Fe2+;
| -2 |
| S |
点评:本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较小.

练习册系列答案
相关题目
下列物质间的转化,能一步实现的是( )
| A、Fe2O3→FeCl2 |
| B、C-H2CO3 |
| C、ZnSO4→CuSO4 |
| D、SO2→Na2SO3 |
分子与原子的主要区别是( )
| A、分子大,原子小 |
| B、分子之间有间隙,原子之间没有间隙 |
| C、在化学变化中,分子能分,原子不能分 |
| D、分子能直接构成物质,原子不能 |
如图所示的实验操作,正确的是( )
A、 取用固体药品 |
B、 加热液体 |
C、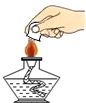 熄灭酒精灯 |
D、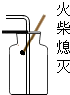 二氧化碳验满 |
下列粒子结构示意图中,表示阳离子的是( )
A、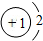 |
B、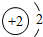 |
C、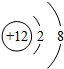 |
D、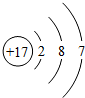 |
下列应用的原理(用化学方程式表示)及基本反应类型均正确的是( )
A、用赤铁矿高炉炼铁Fe2O3+3CO
| ||||
| B、验证铜的活动性比银强Cu+2AgNO3═Cu(NO3)2+2Ag↓ 置换反应 | ||||
C、用天然气作燃料CH4+2O2
| ||||
| D、不能用铁通配制农药波尔多液,因为Fe+CuSO4═FeSO4+Cu 置换反应 |
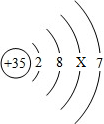 如图是溴(Br)原子的机构示意图,X的值为
如图是溴(Br)原子的机构示意图,X的值为