题目内容
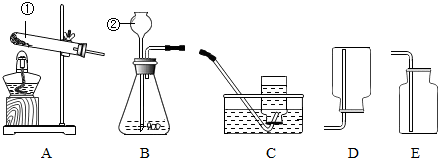
10.在一节化学实验探究课上,张老师拿出两瓶无标签的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究: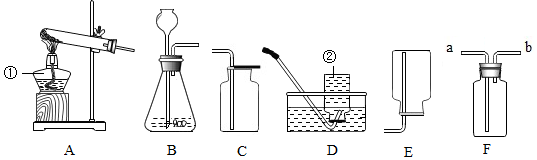
(1)我猜想此气体是氧气.
(2)产生此气体的化学方程式可能是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)我验证此气体的方法是将带火星的木条伸进集气瓶内,观察木条复燃,则是氧气;
(4)我想制取该气体,采用的发生装置可选取如图中的B(填序号,下同),若要收集较为纯净的该气体最好选用装置D.
(5)F是一种可用于集气、洗气等的多功能装置.若将F装置内装满水,再连接量筒,就可以用于测定不溶于水且不与水反应的气体体积,则气体应从b(填“a”或“b”)进入F中.
分析 根据固体和液体产生的气体以及气体的性质进行猜想和验证,根据多功能瓶的作用进行分析解答即可.
解答 解:(1)使用固体和液体产生气体,可能是产生了氧气,故填:氧气;
(2)过氧化氢在二氧化锰的催化作用下分解生成氧气,故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)要检验是否是氧气,可以将带火星的木条伸进集气瓶内,观察木条复燃,则是氧气,故填:将带火星的木条伸进集气瓶内,观察木条复燃,则是氧气;
(4)要使用过氧化氢溶液和二氧化锰制取氧气,则是固液常温型反应,故选择装置B,收集较为纯净的氧气,最好使用排水法,故填:B;D;
(5)将F装置内装满水,再连接量筒,就可以用于测定不溶于水且不与水反应的气体体积,则气体应从b端进入,故填:b.
点评 此题考查的知识点较多,包括气体的制取、发生装置、收集装置的选择等.解决问题时要抓住实验的目的、实验的操作、实验的过程、实验的现象等方面,从基础入手,融汇贯通.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
12.关于碳的燃烧,下列说法中不正确的是( )
| A. | 价值不菲的钻石、默默无闻的碳棒,在氧气中充分燃烧后,产物都是CO2 | |
| B. | 碳和氧气的质量比不同,燃烧产物可能不同 | |
| C. | 碳在充分燃烧时放热,不充分燃烧时吸热 | |
| D. | 碳在氧气中燃烧的产物有可能是混合物 |
5.保持氢气化学性质的最小微粒是( )
| A. | H2 | B. | H | C. | H+ | D. | H2O |
2.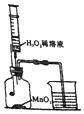 如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验,已知:白磷的着火点为40℃,2NaOH+CO2═Na2CO3+H2O.
如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验,已知:白磷的着火点为40℃,2NaOH+CO2═Na2CO3+H2O.
(1)H2O2稀溶液与MnO2接触时发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2.
(2)实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是燃烧匙中白磷不燃烧是因为未达到白磷的着火点;水中白磷不燃烧是因为没有与氧气接触;推入H2O2溶液后,观察到烧杯中的现象是导管口有气泡冒出,白磷燃烧.
(3)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是支持燃烧;木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶,该实验中,集气瓶内压强的变化过程是先增大后减小.
 如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验,已知:白磷的着火点为40℃,2NaOH+CO2═Na2CO3+H2O.
如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验,已知:白磷的着火点为40℃,2NaOH+CO2═Na2CO3+H2O. | 内容步骤 | [实验1]研究燃烧条件 | [实验2]研究氧气性质 |
| Ⅰ | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞 | 烧杯中盛有NaOH溶液,燃烧匙中放入木炭,点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞 |
| Ⅱ | 推入适量H2O2溶液 | 推入适量H2O2溶液 |
(2)实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是燃烧匙中白磷不燃烧是因为未达到白磷的着火点;水中白磷不燃烧是因为没有与氧气接触;推入H2O2溶液后,观察到烧杯中的现象是导管口有气泡冒出,白磷燃烧.
(3)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是支持燃烧;木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶,该实验中,集气瓶内压强的变化过程是先增大后减小.
19.下列物质的变化中属于化学变化的是( )
| A. |  水果榨汁 | B. |  分离液体空气 | C. |  冰雪融化 | D. |  葡萄酿酒 |
20.化学科学为人类文明和社会进步作出了巨大贡献,下列认识中错误的是( )
| A. | 化学科学的发展为人类研制新材料提供了保证 | |
| B. | 我国歼20飞机、神舟飞船和航空母舰等装备的研制与化学科学无关 | |
| C. | 化学工业是把双刃剑,在提升人们生活品质的同时,也可能会造成环境污染 | |
| D. | 开发利用氢能、太阳能和潮汐能,符合低碳生活理念 |
 依据如图氧化汞分子分解示意图回答问题.
依据如图氧化汞分子分解示意图回答问题.