题目内容
12.有两瓶无色溶液装在没有标签的试剂瓶中,只知道是稀硫酸和稀氢氧化钠溶液.请设计一种实验方案,将它们鉴别开来.写出操作、现象及结论.分析 稀硫酸为酸溶液,氢氧化钠溶液为碱溶液,两者的性质差别很大,因此鉴别这两种无色溶液的方法有许多,根据酸、碱的化学性质的不同进行分析设计实验即可.
解答 解:稀硫酸能使紫色石蕊溶液变红,而氢氧化钠能使紫色石蕊溶液变蓝;氢氧化钠能使无色酚酞变红,而稀硫酸不能使无色酚酞溶液变色;镁、铁等活泼金属能与稀硫酸反应,有气泡产生,而氢氧化钠不与金属反应;还可选用硫酸铜、氯化铁、氯化钡等盐的溶液;还可选用碳酸钠溶液,碳酸钠溶液与稀硫酸反应产生气体,与氢氧化钠溶液不反应,无明显变化.
故答案为:分别取两种溶液少许于两支洁净的试管中,分别滴加无色的酚酞溶液,能使酚酞溶液变红色的是氢氧化钠溶液,无明显变化的是稀硫酸(合理均可).
点评 本题难度不大,属于物质的鉴别题,在解答此类题时,需要选用能与所鉴别物质发生反应且出现明显不同现象的试剂,能反应但无现象的试剂不适合用于物质的鉴别.

练习册系列答案
相关题目
2.以下实验操作中,正确的是( )
| A. | 给玻璃仪器加热时,均垫上石棉网 | |
| B. | 过滤时,将待过滤的混合物直接倒入漏斗中 | |
| C. | 将氢氧化钠固体放在烧杯里进行称量 | |
| D. | 先在试管中加入稀盐酸,再放入锌粒 |
20.二氧化碳的下列用途没有利用其化学性质的是( )
| A. | CO2 用作气体肥料 | B. | CO2 用于灭火 | ||
| C. | 干冰用于人工降雨 | D. | CO2用来制纯碱释 |
7.判断镁条燃烧是化学变化的依据的现象是( )
| A. | 剧烈燃烧,发出耀眼的白光 | B. | 放出大量的热 | ||
| C. | 生成了白色固体 | D. | 生成了氧化镁 |
17.以实验事实和化学原理为依据进行科学推理是学习化学的重要方法之一,下列推理得出的相关结论正确的是( )
| A. | 气体的溶解度随压强增大而增大,所以CO2、SO2的溶解度随压强的增大而增大 | |
| B. | 酸电离出的阳离子是H+,NaHSO4能电离出H+,所以NaHSO4是酸 | |
| C. | 碱性氧化物和水反应生成碱,所以氧化铁与水反应可生成氢氧化铁 | |
| D. | 酸碱指示剂可用于检测溶液酸碱性,所以可用无色酚酞溶液区分盐酸、烧碱溶液和水 |
18.工业上常利用电石制乙炔气体(C2H2)时产生的灰浆和残渣制备化工原料KClO3和超细CaCO3.
电石制乙炔气体(C2H2)时产生灰浆和残渣的过程如下:电石(CaC2)$\stackrel{水}{→}$灰浆$\stackrel{露置于空气}{→}$残渣
其中电石与水反应生成氢氧化钙和乙炔,该反应的化学方程式为:CaC2+2H2O═Ca(OH)2+C2H2↑
残渣中主要成分是Ca(OH)2和CaCO3.
Ⅰ.制备KClO3的流程如图1所示:
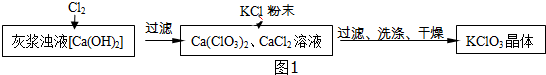
(1)向灰浆浊液中通入Cl2,得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O.
(2)有关物质在常温下的溶解度如表:
上述流程中加入KCl粉末,KCl与Ca(ClO3)2(填化学式)发生了复分解反应,得到KClO3晶体.你认为能得到KClO3 晶体的原因是相同温度下,氯酸钾的溶解度小.
(3)洗涤时,可以选用下列BC作洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如图2所示(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):
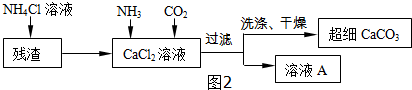
(4)流程中溶液A可循环使用,其主要成分的化学式是NH4Cl.
电石制乙炔气体(C2H2)时产生灰浆和残渣的过程如下:电石(CaC2)$\stackrel{水}{→}$灰浆$\stackrel{露置于空气}{→}$残渣
其中电石与水反应生成氢氧化钙和乙炔,该反应的化学方程式为:CaC2+2H2O═Ca(OH)2+C2H2↑
残渣中主要成分是Ca(OH)2和CaCO3.
Ⅰ.制备KClO3的流程如图1所示:

(1)向灰浆浊液中通入Cl2,得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O.
(2)有关物质在常温下的溶解度如表:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(3)洗涤时,可以选用下列BC作洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如图2所示(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):

(4)流程中溶液A可循环使用,其主要成分的化学式是NH4Cl.
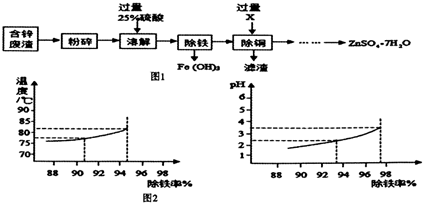
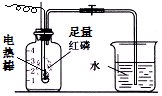 按如图组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题:
按如图组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题: