题目内容
4.在100g双氧水中加入0.5g二氧化锰,完全反应后溶液的质量为96.8g(假设产生的气体全部逸出).(1)反应生成气体的质量是3.2g.
(2)双氧水中过氧化氢的质量分数为多少?
分析 过氧化氢在二氧化锰的催化作用下分解生成水和氧气,反应前后的质量差即为反应生成氧气的质量,根据氧气的质量可以计算过氧化氢的质量,进一步可以计算该双氧水溶液中质量的质量分数.
解答 解:(1)反应生成氧气的质量为:100g-96.8g=3.2g,
故填:3.2;
(2)设过氧化氢的质量为x,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
68 32
x 3.2g
$\frac{68}{x}=\frac{32}{3.2g}$,
x=6.8g,
该双氧水溶液中质量的质量分数为:$\frac{6.8g}{100g}$×100%=6.8%,
答:该双氧水溶液中质量的质量分数为6.8%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
14.下列实验方案不合理的是( )
| A. | 用碘水检验面包片中含有淀粉 | |
| B. | 用闻气味的方法鉴别氢气和氧气 | |
| C. | 用取样灼烧的方法鉴别羊毛和合成纤维 | |
| D. | 用氯化钡溶液鉴别稀盐酸和稀硫酸 |
15.下列自行车的防锈方法不合理的是( )
| A. | 车架--烤漆 | B. | 辐条--镀防护金属 | ||
| C. | 轮圈--烤蓝(表面形成致密氧化膜) | D. | 把手--涂防锈油 |
12.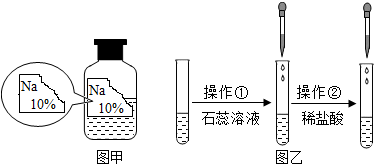 某同学在实验室发现了一瓶标签残缺的无色溶液(如图甲所示),为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题.
某同学在实验室发现了一瓶标签残缺的无色溶液(如图甲所示),为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题.
【猜想与假设】溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种.
【资料查阅】上述四种物质的相关信息如表:
【探究过程】如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是石蕊试液变成蓝色;在进行操作②时有无色无味的气体产生,由此又可排除假设物质中的氢氧化钠.
【探究结论】你认为该溶液中的溶质可能是上述假设物质中的碳酸钠,你的判断依据是碳酸氢钠饱和溶液的质量分数不可能达到10%,而碳酸钠溶液可以.
【探究反思】若上述探究结论是正确的,操作②产生的气体应是CO2(写化学式),实验室检验该气体的实验操作及现象是将气体通入石灰水,石灰水变浑浊.
 某同学在实验室发现了一瓶标签残缺的无色溶液(如图甲所示),为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题.
某同学在实验室发现了一瓶标签残缺的无色溶液(如图甲所示),为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题.【猜想与假设】溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种.
【资料查阅】上述四种物质的相关信息如表:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
【探究结论】你认为该溶液中的溶质可能是上述假设物质中的碳酸钠,你的判断依据是碳酸氢钠饱和溶液的质量分数不可能达到10%,而碳酸钠溶液可以.
【探究反思】若上述探究结论是正确的,操作②产生的气体应是CO2(写化学式),实验室检验该气体的实验操作及现象是将气体通入石灰水,石灰水变浑浊.
19.下列是有关物质的俗名,不含钙元素的是( )
| A. | 生石灰 | B. | 石膏 | C. | 大理石 | D. | 火碱 |
16.物质性质决定用途.下列说法错误的是( )
| A. | 干冰升华吸热,用于制造舞台云雾 | |
| B. | 硫酸铜溶液能与铁反应,用于湿法炼铜 | |
| C. | 熟石灰具有碱性,和化肥硫酸铵混合使用改良酸性土壤 | |
| D. | 镁能在空气中燃烧发出耀眼的白光,可用于制造照明弹 |
13.将等质量等质量分数的烧碱溶液和稀盐酸混合充分反应后,下列各物质不能与混合后的溶液反应的是( )
| A. | CO2 | B. | Mg | C. | AgNO3 | D. | Cu(OH)2 |
14.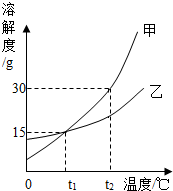 甲、乙两种固体的溶解度曲线如图所示,下列说法不正确的是( )
甲、乙两种固体的溶解度曲线如图所示,下列说法不正确的是( )
 甲、乙两种固体的溶解度曲线如图所示,下列说法不正确的是( )
甲、乙两种固体的溶解度曲线如图所示,下列说法不正确的是( )| A. | t1时,甲、乙两物质各50g分别加入l00g水中,充分溶解,得到的溶液质量都是115g | |
| B. | t1时,甲、乙溶液中溶质的质最分数一定小于15% | |
| C. | t2℃时,将甲、乙的饱和溶液降温至t1℃,甲析出的固体质量一定大于乙 | |
| D. | t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数 |