题目内容
12. 钠摄入过量或钾摄入不足都是导致高血压的风险因素.日常生活中选择食用低钠盐能实现减钠补钾.如图为某品牌低钠盐的标签,请你根据标签回答以下问题:
钠摄入过量或钾摄入不足都是导致高血压的风险因素.日常生活中选择食用低钠盐能实现减钠补钾.如图为某品牌低钠盐的标签,请你根据标签回答以下问题:(1)低钠盐是B(填序号,A:纯净物 B:混合物)
(2)氯化钾(KCl)的相对分子质量为74.5.
(3)人体每天摄入钠元素的质量不宜超过2.3g.如果人体所需的钠元素全部来自该品牌的氯化钠(NaCl),那么一个人每天摄入该品牌低钠盐的质量不宜超过多少克?(结果保留一位小数)
分析 (1)根据低钠盐的组成来分析;
(2)相对分子质量为分子中各原子的相对原子质量总和;
(3)如果已知氯化钠中的钠元素的质量,可以计算氯化钠的质量.
解答 解:(1)由标签信息可知,低钠盐是由氯化钠和氯化钾组成的,属于混合物,故填:B;
(2)氯化钾的化学式为KCl可知氯化钾的相对分子质量=39+35.5=74.5;故填:74.5;
(3)设一个人每天摄入该品牌低钠盐不宜超过的质量x
x×70%×($\frac{23}{23+35.4}×100%$)=2.3g
x=8.4g
答:一个人每天摄入该品牌低钠盐是质量不宜超过8.4g.
点评 根据化学式可以表示物质的组成与构成,利用物质的化学式进行计算.

练习册系列答案
相关题目
2.英国科学家法拉第在《蜡烛的故事》系列讲座中,对蜡烛燃烧所涉及的知识进行了全面介绍.生产蜡烛的主要原料是石蜡和少量的硬脂酸添加剂等有机物,现在让我们一起对蜡烛原料的组成元素进行探究.
【提出问题】生产蜡烛的原料中主要有哪些元素?
【假设与猜想】一定有含碳、氢两种元素,可能含氧元素.
【设计实验】
【分析与交流】
实验步骤(1)和(2)获得的证据均不能证明原料中一定存在氧元素,因为反应物有氧气,因此无法判断原料中是否含有氧元素.
【提出问题】生产蜡烛的原料中主要有哪些元素?
【假设与猜想】一定有含碳、氢两种元素,可能含氧元素.
| 实验步骤 | 实验现象 | 结论 |
| (1)在蜡烛火焰上方放置干冷的烧杯. | 烧杯内壁有小水珠 | 原料中一定存在(填元素符号)H. |
| (2)在蜡烛火焰上方罩一个内壁附着有澄清石灰水的烧杯,观察现象. | 石灰水变浑浊 | 原料中一定存在(填元素符号)C. |
【分析与交流】
实验步骤(1)和(2)获得的证据均不能证明原料中一定存在氧元素,因为反应物有氧气,因此无法判断原料中是否含有氧元素.
3.检验H2纯度时,用排水法收集一试管气体,移到酒精灯火焰上点燃时,没有听到声音,下列原因中,最不可能的是( )
| A. | 氢气已经纯净 | B. | 点燃时试管口离火焰太远 | ||
| C. | 移动试管过程中漏气 | D. | 气体在试管中储存时间过长 |
4.下列物质用途错误的是( )
| A. |  用盐酸制药物 | B. |  用钛合金制造人造骨 | ||
| C. |  活性炭炼铁 | D. |  硫酸用于汽车铅酸蓄电池中 |
2.向量筒中注入水,俯视读数为20毫升,倒出一部分水后,仰视读数为5毫升,则实际倒出来的水的体积( )
| A. | 肯定大于15毫升 | B. | 肯定少于15毫升 | C. | 肯定等于15毫升 | D. | 无法确定 |

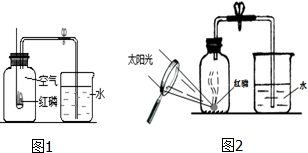 在“空气中氧气含量的测定”实验探究中,甲生设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如下图所示)回答下列问题:
在“空气中氧气含量的测定”实验探究中,甲生设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如下图所示)回答下列问题: