题目内容
7.某硫酸亚铁、硫酸铁的混合物,测得其中含硫24%,求混合物中氧元素的质量分数48%.分析 根据硫酸根中硫元素与氧元素的质量比,再求氧元素的质量分数,进行分析解答.
解答 解:根据硫酸根中硫元素与氧元素的质量比为:32:(16×4)=1:2;混合物中含硫24%,依据质量分数的求法,可知混合物中氧元素的质量分数为:2×24%=48%,故答案为:48%.
点评 本题考查学生利用质量分数灵活应用进行分析解题;计算时要理清各个量之间的关系,再结合题意进行分析解答.

练习册系列答案
相关题目
12.下列化学符号中数字“2”表示的意义不符合的是( )
| A. | 2NH4+:二个铵根离子 | |
| B. | H2O:一个水分子中含有一个氢分子 | |
| C. | Mg2+:一个镁离子带二个单位的正电荷 | |
| D. | $\stackrel{+2}{Cu}$O氧化铜中铜元素的化合价为正二价 |
19.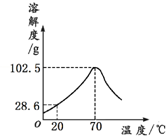 甲物质的溶液可用作化肥、电镀液等.甲的溶解度曲线如图所示,下列说法正确的是( )
甲物质的溶液可用作化肥、电镀液等.甲的溶解度曲线如图所示,下列说法正确的是( )
 甲物质的溶液可用作化肥、电镀液等.甲的溶解度曲线如图所示,下列说法正确的是( )
甲物质的溶液可用作化肥、电镀液等.甲的溶解度曲线如图所示,下列说法正确的是( )| A. | 甲的溶解度随温度的升高而增大 | |
| B. | 20℃时,100 g甲的饱和溶液中溶质质量为28.6 g | |
| C. | 将70℃甲的饱和溶液升高温度,有晶体析出 | |
| D. | 70℃时,甲的饱和溶液的溶质质量质量分数为50.6% |
17.下列变化过程中只发生了物理变化的是( )
| A. | 生石灰做干燥剂 | B. | 废气中的二氧化硫形成酸雨 | ||
| C. | 由氮气和氢气合成氨气 | D. | 二氧化碳气体制成干冰 |