题目内容
19.将25g石灰石(主要成份是 CaCO3)放入100g稀盐酸中(石灰石中的杂质不跟盐酸反应,也不溶于水)恰好完全反应,生成4.4g二氧化碳气体.试求:(1)石灰石中碳酸钙的质量分数;
(2)稀盐酸中溶质的质量分数;
(3)反应后溶液中溶质的质量分数.
分析 根据碳酸钙与盐酸反应的化学方程式,由生成的二氧化碳的质量求出碳酸钙、盐酸溶液中的溶质、生成的氯化钙的质量,在计算出石灰石中碳酸钙的质量分数、稀盐酸中溶质的质量分数和生成氯化钙的质量,进而计算出反应后溶液中溶质的质量分数.
解答 解:设石灰石中碳酸钙的质量为x,稀盐酸中溶质的质量为y,生成氯化钙的质量为z.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 111 44
x y z 4.4g
$\frac{100}{x}$=$\frac{73}{y}$=$\frac{111}{z}$=$\frac{44}{4.4g}$
解得:x=10g y=7.3g z=11.1g
(1)石灰石中碳酸钙的质量分数为:$\frac{10g}{25g}$×100%=40%;
(2)稀盐酸中溶质的质量分数为:$\frac{7.3g}{100g}$×100%=7.3%;
(3)反应后溶液中溶质的质量分数为:$\frac{11.1g}{25g+100g-4.4g}$×100%=9.2%.
答:(1)石灰石中碳酸钙的质量分数为80%;
(2)稀盐酸中溶质的质量分数为20%;
(3)反应后溶液中溶质的质量分数为9.2%.
点评 本题主要考查含杂质物质的化学方程式计算和溶质质量分数的计算,在计算时,要正确地根据质量守恒定律计算反应的溶液的质量,难度较大.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
9.乙醇是一种常见的燃料,下列有关乙醇的说法正确的是( )
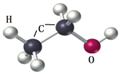

| A. | 乙醇分子是一种化合物 | |
| B. | 乙醇分子是由碳、氢、氧三种原子构成 | |
| C. | 乙醇中氢元素的质量分数最大 | |
| D. | 乙醇中碳元素和氧元素的质量比为2:1 |
10.某学生在量取液体时,量取了20mL水,第一读数时眼睛与凹液面的最低处保持水平,当倒出一部分水后,俯视凹液面的最低处,这时读数是15mL,则该同学倒出的水的体积为( )
| A. | 等于5 mL | B. | 大于5mL | C. | 小于5mL | D. | 无法确定 |
14.下列四个图象分别对应四种操作过程,其中不正确的是( )
| A. |  向NaOH溶液中加水 | |
| B. |  氯酸钾受热分解 | |
| C. |  向等体积、等浓度稀盐酸中加入足量金属 | |
| D. |  往氯化钠溶液中加入硝酸银 |
4.下列物质的性质属于化学性质的是( )
| A. | 颜色 和状态 | B. | 密度 | C. | 溶解性 | D. | 可燃性 氧化性 |
11.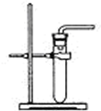 在实验室里同学们用过氧化氢溶液与二氧化锰混合制取氧气(装置如右图).某小组甲、乙、丙三名同学用该装置进行实验过程中,橡皮塞突然被弹飞,并有少量的液体溅到实验台和衣服上.就此异常现象这三名同学进行了如下探究:
在实验室里同学们用过氧化氢溶液与二氧化锰混合制取氧气(装置如右图).某小组甲、乙、丙三名同学用该装置进行实验过程中,橡皮塞突然被弹飞,并有少量的液体溅到实验台和衣服上.就此异常现象这三名同学进行了如下探究:
【问题】橡皮塞为什么会突然弹飞?
【查阅资料】①容器内瞬间产生气体过多,压强过大,可能导致橡皮塞弹飞.
②化学反应速率与反应物的浓度、用量、接触面积、温度、催
化剂等因素有关.
【猜想】甲同学:导气管堵塞造成.
乙同学:过氧化氢溶液用量过多造成.
丙同学:过氧化氢溶液的浓度过大造成.
…
【分析验证】针对以上三种猜想,通过检查实验装置发现导气管没有堵塞的情况;在与其他实验成功的小组交流时,得知各小组所用的过氧化氢溶液的浓度均相同.于是他们否定了甲和丙同学的猜想.请你设计实验,验证另一名同学的猜想是导致本次实验橡皮塞弹飞的可能原因.
【交流反思】(1)老师提示他们引起此实验过程中橡皮塞被突然弹飞的原因可能还有其他因素,老师建议还可进一步探究.而就目前的原因,可以通过改进气体发生装置和操作的方法,避免橡皮塞被弹飞.你对气体发生装置有何改进设想?请你提出改进方法,
【改进方法】.
【问题拓展】
(1)实验结束后,有的同学发现衣服和手上出现白色的斑点.由此推出过氧化氢溶液具有腐蚀性(或氧化性、漂白性)性质.
 在实验室里同学们用过氧化氢溶液与二氧化锰混合制取氧气(装置如右图).某小组甲、乙、丙三名同学用该装置进行实验过程中,橡皮塞突然被弹飞,并有少量的液体溅到实验台和衣服上.就此异常现象这三名同学进行了如下探究:
在实验室里同学们用过氧化氢溶液与二氧化锰混合制取氧气(装置如右图).某小组甲、乙、丙三名同学用该装置进行实验过程中,橡皮塞突然被弹飞,并有少量的液体溅到实验台和衣服上.就此异常现象这三名同学进行了如下探究:【问题】橡皮塞为什么会突然弹飞?
【查阅资料】①容器内瞬间产生气体过多,压强过大,可能导致橡皮塞弹飞.
②化学反应速率与反应物的浓度、用量、接触面积、温度、催
化剂等因素有关.
【猜想】甲同学:导气管堵塞造成.
乙同学:过氧化氢溶液用量过多造成.
丙同学:过氧化氢溶液的浓度过大造成.
…
【分析验证】针对以上三种猜想,通过检查实验装置发现导气管没有堵塞的情况;在与其他实验成功的小组交流时,得知各小组所用的过氧化氢溶液的浓度均相同.于是他们否定了甲和丙同学的猜想.请你设计实验,验证另一名同学的猜想是导致本次实验橡皮塞弹飞的可能原因.
| 实验步骤 | 实验现象 | 结论 |
【改进方法】.
【问题拓展】
(1)实验结束后,有的同学发现衣服和手上出现白色的斑点.由此推出过氧化氢溶液具有腐蚀性(或氧化性、漂白性)性质.
8.下列化学用语中既能表示一种物质,也表示组成这种物质的元素,还能表示该元素的一个原子的是( )
| A. | N2 | B. | Fe | C. | H | D. | Mg2+ |